さあ、今日の記事はなかなかのボリュームになることが予想されます。
最初にお断りしておきますが、化学基礎とかで出てくるような、強酸の水素イオン濃度の求め方とはレベルが違います。
センターで、化学基礎しか使わないというような迷い込んで来た、文系ちゃんはこのページを閉じてyoutubeでUVERworldでも聞いていましょう。
さあ!残った理系諸君!覚悟はいいですか?このpH計算は本当に、
面倒くさい!
「強酸は水の電離を考える場合、考えない場合がある!」
「弱酸は電離定数Kaを考える必要がある!」
「厳密解と近似解がある!」
「弱酸のときは、電離度αをつかって近似解が使えるか判定?」

どんだけあんねん!!!
だから、今回の記事では、pH計算のための水素イオン濃度を最悪暗記せずに求められる方法をお教えします!
あるから、その都度この記事みながら、
紙を用意して
俺がどのようにして水素イオン濃度を求めているかマスターして行ってくだされ。
これが出来たら多くの受験生と大幅に差を付けられるから、あきらめずに最後まで読んでいってくださいね!
目次
水の電離について!〜イオン積とは?〜
水素イオン濃度を求める場合、水の電離を考えるか否か?ということが関わってくるから、水の電離自体を知っておく必要があります!
水の電離反応は可逆反応!
水の電離反応は、下のような反応式となる。
H2O⇄H++OH–
となり、可逆反応である!
可逆反応は、両方残るので、左辺も右辺ものこります。これはわかりますよね。もし、水の電離が不可逆反応だったら、
琵琶湖今頃無くなってますよね(笑)
琵琶湖がまだまだ日本一の湖として残っているのは、水の電離が可逆反応だからです。つまり化学平衡の法則を使えるので、水の電離平衡状態の平衡定数を求める事が出来ます。
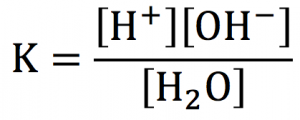
水溶液中の[H2O]
水溶液中の[H2O]は下の計算式で求める事が出来ます。
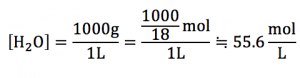
と、『メチャクチャデカい』値になる。
だから、水溶液中のH2Oが多少反応に使われたとしても、その濃度はほぼかわらない。
純粋の電離についてモル濃度収支を取ると、下表のようになります。

このように水の電離で減少するH2Oのモル濃度は鼻くそレベル。

よって[H2O]は定数と見なせます!そこで、偉い人は考えました。
平衡定数と一緒にしちゃえ!
この[H2O]を両辺に掛けて、左辺はK×[H2O]となりました。K×[H2O]をKWとおき、これを水のイオン積としました。
つまり、
水のイオン積は平衡定数の一種
というわけなのです。
ということは、平衡定数は温度に依存しますから、水のイオン積も温度で変化します。水の電離は、下のような吸熱反応で表されます。
H2O⇄H++OH–-QkJ(Q>0)
勘のいいあなたなら分かるでしょう。ルシャトリエの原理より、温度が上がると吸熱方向に平衡は移動するので、
上式の平衡は右へ傾き、[H+]、[OH–]の濃度は高くなります。
すると、水のイオン積も大きくなります。普段使っている、水のイオン積は、
KW=1.0×10-14(mol/L)2は、
熱化学の標準状態(25℃、1atm)のときの値であり、
60℃位まで温度が上がると、KW=1.0×10-13(mol/L)2に変化します!
電離定数とは?
まず、電離平衡の話をする前に、電離定数というものを解説しておこうと思います。電離定数は平衡定数の一種なので、高校化学レベルでは弱酸弱塩基にしか存在しません(厳密にいうと強酸のレベルによっても違いがあるんですがね。)
電離定数とは、弱酸弱塩基の平衡定数を少し加工したものです。使い方や性質はほとんど平衡定数と一緒なんですが、この電離定数はちょっと違います。
中性条件とpH
中性とは、水溶液中で[H+]=[OH–]の状態の事を言います。
だから、水のイオン積KWが水温によって変化するので、中性を示すpHも温度により変化します。
先ほど言ったように、60℃でのKW=1.0×10-13(mol/L)2なので、[H+]は、
[H+]=√[KW]=1.0×10-6.5∴pH=-log[H+]=-log(1.0×10-6.5)=6.5
pH計算の公式は-log10[H+]です。
これは定義なので知っとくしかないです。
近似法
この水素イオン濃度を求めるうえで確実に必要なのが、近似法なのです。近似についての考え方をきっちりマスターしておきましょう!
どういう場面で近似出来るか?ということを徹底的に分かっておかないと、強酸の[H+]を求めるときに、水の電離をかんがえるかどうかを考える上で確実に必要になります。
pH計算([H+]計算)は厳密解を計算すると複雑すぎるケースが多々ありますので、近似解にすることが多い。
①近似の仕方
よく、>>こういう不等号見ませんか?a>>bこれは、aの方がbよりもめちゃくちゃでかいっていう意味なんですが、これを見つけた時は、a+b≒aという風に扱っていいよ!ってことなんです。
これを近似と言います。近似は、 足し算、引き算の時に、A>>Bだったとすると、A:B=100以上:1なら、Bを無視できます。

つまり相対的に小さい物を省くと言う物が近似法です!
注意点
掛け算割り算は、近似で無視することはできません。これができてしまったら、例えば気体の分野で問題文の条件で「1.0×105Paとする」と書いてあったとして、
1.0×105=10×104=104
つまり105=104
みたいな意味不明なことになりますからね。なので掛け算割り算では使えません。
例題!
297×101
という式があったとします。この時に、普通にやるのではなく近似を使えばこんな感じになります。
(300-3)×(100+1)≒300×100=30000
という風に近似計算できます。
実際、297×101=29997ですから、29997=30000-3≒30000です。この近似は酸塩基のpHを求める上でめちゃくちゃ重要です。
強酸や強塩基の[H+]濃度の求め方
さあ早速具体的に水素イオン濃度[H+]の計算をして行きます。
厳密解を考える場合、[H+]をもとめるには、正確に水の電離も考慮しなければなりません。そのときは、『水のイオン積KW』も考慮します。
ここで受験テクニックをお教えします。こういう[H+]計算では、必ずやらなければならない事があります。
これさえできれば、「こういうときは、この式使って、こういうときは、この式、、」
これさえすればその場で必ず導きだせるので、式を間違って失点する事が無くなります。
しかし、このテクニックを軽視して、丸暗記に走ってしまうと、本当に頭の中がごちゃごちゃになって、覚え違いで点数を失うと言う超ださい間違え方をしてしまいます。
なのでこのテクニックは目ん玉かっぽじってキッチり学んでください!
そのテクニックとは、
『図を書く』
というテクニックです。
受験化学コーチなかむらがいろんなところで使うテクニックですね!気体でも使いましたし、濃度計算でもしましたね!
これは、本当に重要です。人間は分からない物を視覚化すると分かりやすくなるので、この図の書き方を学んで行けば水素イオン濃度くらい毎回手動で求めることができます。
厳密解
まず強酸の厳密解は下のような図を書けば分かります。

例としてHClをつかっていますが、HClは強酸なので、電離は不可逆で、電離定数Kaは考慮する必要がありません。
Camol/LのHClは水溶液中で完全に電離し、Camol/LのH+を生じる。
が、HCl中の[H+]の厳密解を求めると言うのは、水の電離によって生じるH+も考慮すると言う事。
水の電離により生じるH+も考慮しH+の濃度の全量をxmol/Lとして、モル濃度の収支を表した図を書くと下図のようになる。

[H+]全量=xmol/L、
[OH–]全量=x-Camol/L、
これをKWの水のイオン積に代入すると、
KW=[H+][OH–]=x×(x-Ca)
この2次方程式を解けば厳密解となります。
よって、

近似解
さきほどお話ししました近似法をフル活用して、『どういうときに近似解をつかえるのか?』を求めて行きます。
先ほど近似出来る場面をお教えしました、近似できるのは、

のときです。
これを今回に適用します!
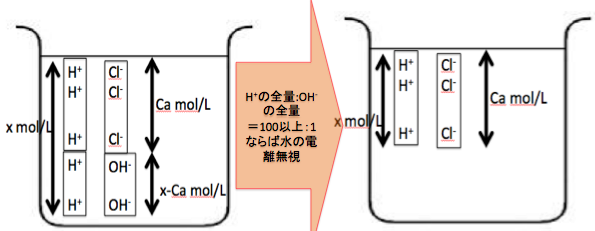
先ほど言いました、H+の全量:OH–の全量=100:1が実現するとき、
[OH–]=x’/100mol/L
であれば無視できますよね!
これを水のイオン積の式に代入します!
KW=x’×x’/100=1.0×10-14
よってX’=1.0×10-6
そして、KW=一定なわけですから、[H+]≧1.0×10-6であれば、近似解を使える、つまり水の電離を無視できるわけです。
強酸の水素イオン濃度の計算法まとめ!
HClaqCamol/Lの場合
HClの電離により生じるH+で
[H+]≧1.0×10-6mol/Lは明白!
∴[H+]=Camol/L
・Ca≦1.0×10-6mol/L
水の電離を考慮して下の図を書きましょう!


例題を出します!
例題 以下のモル濃度のHClaq中の
[H+]を計算せよ。
1)HClaq0.010mol/L
→0.01mol/L>1.0×10-6mol/Lなので、
水の電離は無視できます。
[H+]=Ca=0.01mol/L
2)HClaq1.0×10-7mol/L
1.0×10-7mol/L<1.0×10-6mol/Lなので、
水の電離を考慮し、
[H+]全量=xmol/Lとして下図を記します。
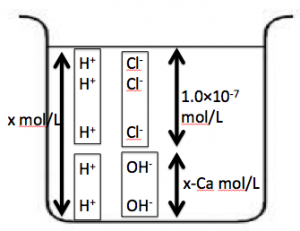
KW=[H+][OH–]
=x(x-1.0×10-7)=1.0×10-14
∴x=[H+]≒1.6×10-7mol/L
強塩基の水素イオン濃度
方針
強塩基であるNaOHなどは、
HCLなどと同様不可逆変化であり、
計算式は強酸と全く同じ形になります!
あだH+がOH–になるため、
添字のa(acid)がb(base)になります。
よって
NaOHの電離により生じるOH–で
[OH–]≧1.0×10-6mol/Lは明白!
∴[OH–]=Cbmol/L・Cb1.0×10-6mol/L
水の電離を考慮して下の図を書きましょう!
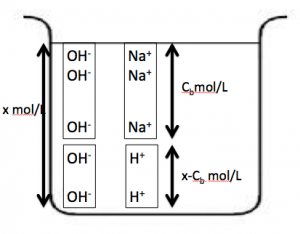
水の電離の考慮の必要とpHの関係性まとめ
水の電離の考慮が必要なのは強酸強塩基のモル濃度は、
[H+]≧1.0×10-6mol/L
つまりpH≧6.0
塩基性水溶液なら
[OH–]≧1.0×10-6mol/L
つまりpH≦8.0
弱酸・弱塩基の水素イオン濃度計算法
1価の弱酸の水素イオン濃度計算
弱酸、今回は酢酸(CH3COOH)を例にします
酢酸の電離反応は以下のようになります
HA⇄H++A–
これは『可逆反応』なので、
電離定数Kaを考慮する必要がある。
AH⇄A–+H+
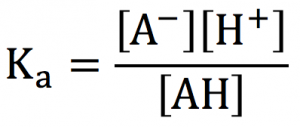
水のイオン積を使って水の電離まで考えると、弱酸の場合、3次方程式までになってメチャクチャ煩雑になるんだ
水のイオン積KWを無視して計算します。

そしてこの事をあなたには賢く使ってほしいのです。まず、弱酸で水の電離を考えるパターンは出ません。
だから、これを逆手に取ってしまえばいいのです。
つまり、あなたが求めた
WAの[H+]計算の問題の解が1.0×10-6より小さい事はありえないと言うわけです!
あなたが計算してもし、[H+]<1.0×10-6となった場合、
『計算ミスです』
やり直してください!
弱酸の厳密解
CH3COOH(AH)Camol/Lのうちxmol/Lが電離したと考えて、モル濃度および水溶液の図を記すと以下のようになります。
強酸と同様に電離した図を書きます。ですが、弱酸なので、全て電離しません。
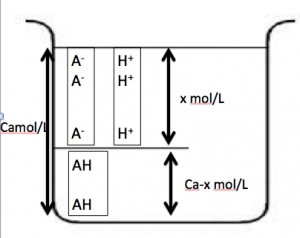
このデータを電離定数に代入します!
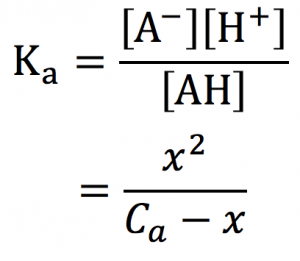
よってこれは2次方程式を解く事で、水素イオン濃度[H+]を求められます
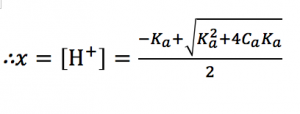
近似解
水の電離は考えませんが、上の解は厳密解です。しかし、弱酸と言うのは、完全に電離するわけではありません。
電離した水素イオン濃度[H+]がCaに対して小さければ、Ca-x=Caと近似できます。x=α×Caですから、Ca-x=Ca(1-α)です。
つまり、電離度がα<<1だったらいいのです。先ほども言いましたが、近似する条件としては、100以上:1なので、電離度αが0.01以下ならば、弱酸の水素イオン濃度は近似解を使うことができます。
ただ、電離定数Kaの値が2~3%の誤差を含むと言われています。。なぜなら電離定数Kaは実験から求めるため、誤差が現れるのです。
なので、だいたい電離度が0.05以下ならば近似解を使えると思ってください。
よって、電離度は全体のうち電離した割合ですので、
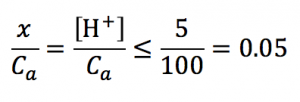
のようになります。
よって、
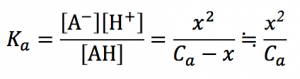
これを解くと
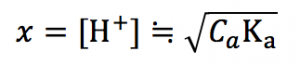
この近似解は公式として覚えておいていいです。
弱酸の[H+]の解法
それでは弱酸の水素イオン濃度求め方を一気にまとめて行きます!
手順まとめ
ステップ1:ひとまず[H+]≒√CaKaで計算
ステップ2:電離度αを確認する。
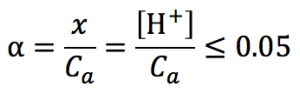
これを満たしているとき→[H+]≒√CaKaの解でオッケー!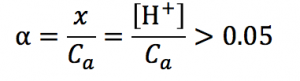
満たさないとき、
→
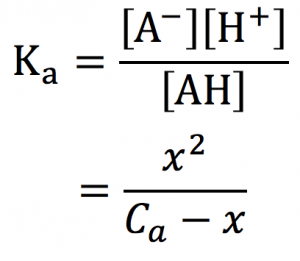
の式を立てて解く。
電離度αの公式を導出!
CH3COOH(AHと省略)の電離に関して電離度を用いて図を書いて行きます!
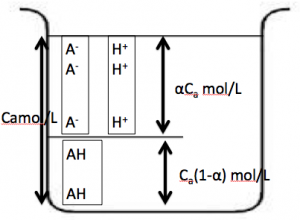
このような電離図を書いて、これを弱酸の電離定数を求める式に代入します
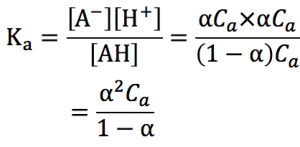
この式を解くと、
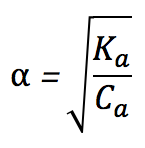
このようになります。このように電離度を求めることもできます。ちなみに、
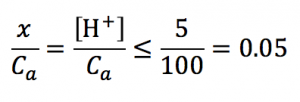
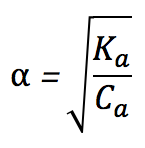
この2つの電離度の公式はどちらを使えばいいのか?と質問が来ますが、電離度を直接計算しなければならない場合は、下の式を使ってください。
なぜなら、上の式は[H+]が問題文で与えられていません。(1)で[H+]を求めて (2)で電離度を求めるとして、(1)の答えを使って(2)を求めると、(1)が間違っていた時に共倒れです。
なので、(2)の与えられているものだけで計算できる方が正答率は高くなります。
2価の弱酸の[H+]の求め方
さあ1価は色々複雑な過程はありましたが、結局は、[H+]=√CaKaというシンプルな形になりました。
それでは2価の弱酸はどのような[H+]はどう表されるのでしょうか。
2価のWA(H2Aとする)は以下の2段階で電離します。
(第1電離)
H2A⇄H++HA–
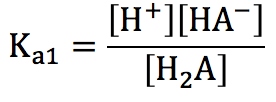
(第2電離)
HA–⇄H++A2-
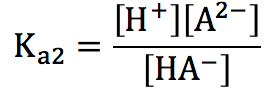
ですが、2価のWAはたいていKa1>>Ka2で、第2電離で生じるH+は微々たる物であるため、
受験で弱酸の第2電離は無視します!
よって、[H+]=√CaKaとなります。
また、このときも
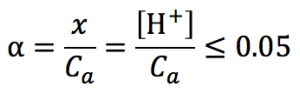
であることを確認してくださいね!
ちなみにいうと、大抵は近似解で解くことができますし、あまりにも微妙な電離度になることはありません。電離度が0.054だから、無視できない!
とかそんなことはなく、0.05よりも電離度が大きくなります。
1価の弱塩基の[H+]の求め方
HCl(強酸)とNaOH(強塩基)の説明はと同様で、弱酸と弱塩基とは電離反応が電離反応が可逆的であると言うことは、同じです。
よって、計算式の形は同じになります!ただ、[H+]は[OH–]に1添字のa(acid)はb(base)に変わります!
これに注意点NH3の電離平衡の法則に適用するとき、水溶液中の[H2O]は前著のように、ほぼ定数と見なせるので、平衡定数を表す式から省くのをキッチリ覚えておいてください。
![]()
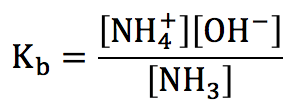
弱塩基のまとめ
2)電離度αを確認する。
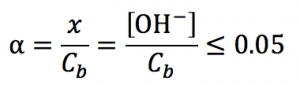
これを満たしているとき
→[OH–]≒√CbKbの解で
オッケー!
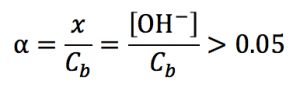
判定式を満たさないとき、
→
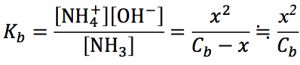
の式を立てて解く。
このような感じで普通の[H+]水素イオン濃度を求めて行きます。
塩の加水分解の[H+]の求め方
塩の加水分解の求め方は実は、ここまで習って来た事を使えます。
しかし、普通に何の背景も知らずに使うのは、危険だから次の記事で俺が話している手順もめちゃくちゃ大事だから。
ちゃんと読んでおいて。
塩の加水分解とは?計算問題が出来ないシンプルすぎる理由は?
緩衝液に置ける[H+]の求め方
【朗報】緩衝液の入試問題の解法が簡単過ぎワロタw原理も解説!
さあ、どうでしょうか?なかなか大変だったかもしれませんが、体系的にまとめてみました。
なるべく解法は頭に入れて欲しいですが、どうしてもできない場合は図を書いて毎回求め直すというのもありです!いや、むしろ慣れるまでは、必ず毎回自分で図をかく癖をつけておいてください。
こちらが動画版になります。






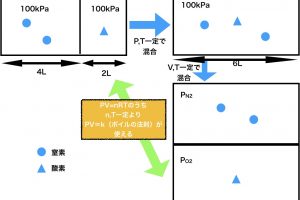









濃度平衡定Kc
圧平衡定数Kp
電離平衡定数Ka,Kb
水のイオン積Kw
溶解度積Ksp
これらの違いってどうやれば分かるんですか?
それぞれの内容を学んで行けばいいのでしょうか?
普通に、勉強して行けば必ず出てきますのでそこで学んで行けばいいです。
KcのCは濃度Concentration
KpのPは圧力pressure
Kaはacid(酸性)
Kbはbase(塩基性)
Kwはwater(水)
Kspはsolibility producet(溶解度 積)
と言う風に英語を覚えれば一発で分かります。
α=[H+]/Caと、α=√Ka/Caの違いがよくわからないです。どういった時に使い分けるんですか?
まあ、直接電離度が問われたらα=√Ka/Ca
そして、チェックするときはα=[H+]/Ca
です。
pH=3の塩酸を純水で10000倍に薄めた溶液のpHはいくらか。というセンサーの問題で塩基性にならない理由がよく分かりません。
炭酸水やお酢を水で薄めても塩基性にはなりません。
水を加えても水酸化物イオンが増えないからです。
電離平衡の根幹となる考え方とかってありますかね?
電離平衡の根幹となる考え方とかってありますか?
実際に図を描いてみるとよくわかりますね!
定期テストの範囲ですが、問題集の問題がかんたんに見えるようになりました!