逆滴定は2パターンありましたが、そのうちの難しい方、二酸化炭素の逆滴定の問題解説に入っていきます。
テキストで逆滴定に関して説明しまくりました。そして、この問題は中和滴定総集編の様な問題です。炭酸ナトリウムの二段滴定からワルダー法までいろんなエッセンスが出まくっているので、きっちりマスターしちゃってくださいね!
指示薬としてフェノールフタレインを浸かったとき塩酸はV1mL、メチルオレンジを浸かったとき塩酸はV2mLで指示薬を変色した。
問1溶液Aに含まれている物質が次の(a)~(d)の場合、それぞれV1とV2の関係を表す式はどれか。下の(1)~(6)から最も適するものを選び、番号で答えよ。
(a)水酸化ナトリウムのみ
(b)炭酸ナトリウムのみ
(c)水酸化ナトリウムと炭酸ナトリウム
(d)炭酸水素ナトリウムと炭酸ナトリウム
(1)V1=2V2
(2)V1=V2
(3)2V1=V2
(4)V1>2V2
(5)2V1>V2
(6)2V1<V2
問2a=50.0mL、C=0.100(mol/L)で滴定したとき、V1=22.1mL,V2=48.4mLであった。NaOH,NaHCO3、Na2CO3,の濃度(mol/L)を有効数字2桁で求めよ。溶液内に含まれていない物質は値は0とせよ。
出典:重要問題集2017 129 福岡大学2012年
この問題の方針
さて、このような問題はなかなか難しいですね。
とにかく混乱しまくる問題は、まずは「図」にして徹底的に理解していきましょう。
HClは今どの物質を滴定しているのかをしっかり理解しておきましょう。
問題の解法!
(a)溶液AがNaOHaqの場合
この問題は強塩基(Strong Base 以下SB)の
NaOHaqをフラスコにいれ、
強酸(Strong Acid 以下SA)である
HClaqをビュレットで滴下した実験です。
結果、pH=7よりかなり数値の大きい
強塩基性から、pH=7よりかなり
数値の小さい強酸性へ移行する
滴定曲線が得られるはずです。
(pHジャンプ)
これに
フェノールフタレイン(pp)と
メチルオレンジ(MO)の変色域を
被せると下のようになる。
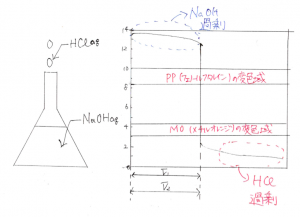
結果、フェノールフタレインが、
変色するまでの体積V1と
メチルオレンジ(MO)が変色
するまでの体積V2は等しくなる。
よってV1=V2
選択肢(2)が正解です。
(b)溶液AがNa2CO3aqの場合
※これ以降の問題では、
逆滴定により、2段階の滴定曲線に
なるため、フェノールフタレイン(pp)の
変色からメチルオレンジの変色まで
ビュレットから滴下した体積をV3として
説明します!
(炭酸ナトリウム)
強塩基+弱酸由来の塩でブレンステッド定義で塩基として働くNa2CO3aqをフラスコにいれ強酸であるHClaqをビュレットで滴下した実験である。
そして、中和滴定の問題は、『滴定曲線を書く』のが方針でした。
そこで、下のような図を書きました。

これからわかることは、
→第1段階の終点は、PPで判明
しました。
→第2段階の終点はMOで判明
しました。
炭酸ナトリウムnsmolをHClaqで滴定するとき、
下図のように片手ずつ中和されて
行きます。

・炭酸ナトリウムnmolをHClnmolが
反応してPPが変色します。
・炭酸ナトリウムnmolが炭酸水素ナトリウムに
nmolに変化し、そのNaHCO3nmolが
HClnmolが反応、MOが変色します。
下のように、炭酸イオンの
片手ずつ、水素イオンをキャッチしていって
反応していくのです。

炭酸ナトリウムの滴定
炭酸ナトリウムnmolに対し
PP変色までに滴下するHClも、
その後MO変色まで加える
HClもともにnmolで等しい。
HClの加える物質量が等しく、
かつその濃度も等しいので
滴定曲線でのHClの滴下量は等しく、
フェノールフタレイン(PP)
が変色するまでの体積V1とフェノールフタレイン(pp)
の変色からメチルオレンジ(MO)の変色まで
ビュレとから滴下した体積V3は等しい。
つまり、V1=V3
よって、フェノールフタレインが変色するまでの
体積V1の2倍がメチルオレンジ(MO)
が変色するまでの体積V2と等しくなる。
∴V2=2V1(問1(b)=(3))
(c)溶液AがNaOHaq+Na2CO3aqの場合
強塩基であるNaOHaqと
強塩基+弱酸由来の塩で、
ブレンステッド説で塩基として働く
Na2CO3aqを
フラスコにいれ、強酸であるHClaqを
ビュレットで滴下した実験である。
これまた、既に説明した滴定曲線となり、
下記を考慮すれば、グラフは下図の
ようになる。
(1)滴定曲線の前半は、溶液中に
残っているNaOHaqの由来のSB性pHのグラフに!
(2)NaOHが中和された後、Na2CO3が
HClで滴定される。
滴定曲線の後半はNa2CO3+HClの
滴定曲線になる。
と言う事でグラフは下図のようになる。
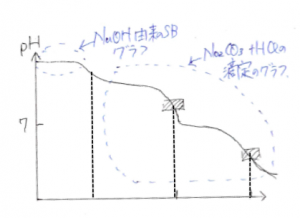
PPの色の変化で下記の2つの反応の
終点が判明する
NaOH+HCl→NaCl+H2O
Na2CO3+HCl→NaHCO3+NaCl
この2つの両方が終わったところで、
PPが赤→無色に変わり、第1段階の反応の
終点になります。
テクニック!
これは、逆滴定をキッチリ滴定曲線を
書いて解いているあなただから
出来る手法です。
それは、
(NaOH+Na2CO3)aq+HClaqの滴定曲線に、
から滴定曲線が始まるであるところに右のように
点線を引く。
という受験テクニックです。
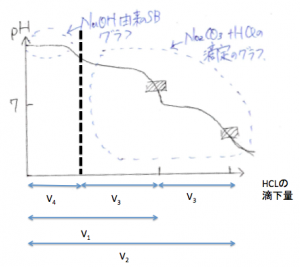
この点線からNa2CO3の滴定が
始まります。
V4はNaOHの滴定で必要だった
HClの滴下量と言えます。
Na2CO3のみなら、PPが変色するまでのHClaqの
滴下量も、PPからMOの変色までビュレットから
滴下するHClaqの滴下量も
等しくV3のはずで、
V1-V3に相当するV4分が
NaOHの滴定に必要な体積!
グラフを見ると分かるように
V1=V3+V4
V2=2V3+V4ゆえ、
V1<V2であるが、
V2=2V1であるためには、
V2=2V3+2V4で
なければならないが、その値よりは、
V2は小さい。
∴2V1>V2(問1(c)=(5))
(d)溶液AがNa2CO3aqの場合
SB+WA由来の塩でブレンステッド則
では塩基として働くNa2CO3aqと
NaHCO3aqをフラスコにいれ、
SAであるHClaqをビュレットで滴下した実験である。
この滴定曲線では、Na2CO3aqのみをHClaqで
滴定する場合と比べ、
その第2段階の滴定がNaHCO3を添加された分
PPの変色からMOの変色まで
ビュレットが滴下するHClaqの量V3は増加する。
・Na2CO3 nsmolをHClaqで滴定するとき
Na2CO3 nsmolにつきHCl nsmolが反応、
PPが変色しNaHCO3 nsmolを生成する。
・そこにNaHCO3 ns‘molを添加すると、
NaHCO3計ns+ns‘molになり、
それをHCl ns+ns‘molで滴定し、
MOが変色する。
滴下するHClの濃度は変わらないので、
PPが変色するNa2CO3nsmolを滴定する
HClの滴下量V1より、
PPの変色から、MOの変色までの
NaHCO3ns+ns‘molを滴定するHClの
滴下量V3の方が多くなるのは自明であろう。
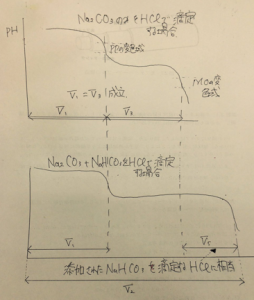
V2=V1+V3でかつV1 < V3
であるからV2はV1の2倍より大きい!
∴V2>2V1(問1(d) (6))
問2溶液A50.0mLを0.100mol/LHClaqで滴定,V1=22.1mL、V2=48.4mLなら?
問題の概要の把握
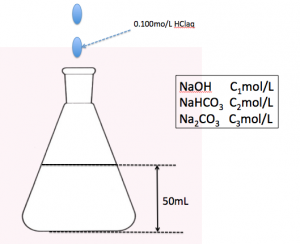
本問は,NaOH(C1mol/Lとする。)、
NaHCO3(C2mol/Lとする)、
Na2CO3(C3mol/Lとする)、
の混合溶液50.0mLを0.100mol/Lの
HClaqで滴定している。
結果、0.100mol/LHClaqの滴下量は、
V1=22.1mL,V2=48.4mLとなっている。
⇒V2/V1=48.4/22.1=2.19・・・>2つまり、
V2>2V1なので、
本問は、(d)のNa2CO3aqとNaHCO3aqを、
強酸であるHClaqで滴下した場合に
相当します。
①NaOHのC1(mol/L)の算出

Na2CO3+NaHCO3aqの混合溶液を
HClaqで滴定していたので、NaOHは
含まれていなかった。
∴C1=0mol/L
NaHCO3のC2mol/Lの算出
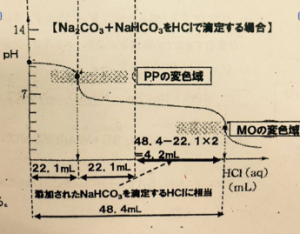
⇒本問がNa2CO3aqのみをHClaqで滴定
するのなら、第1段階の滴定でPPが変色する
までの体積が
V122.1mLなので、
第2段階の滴定でPPの変色からMOの変色までに
必要な体積もV3=22.1mLのはずです。
しかし、第2段階の滴定に必要な0.100mol/L
HClaqの量は、
48.4-22.1×2=4.2mL増加している。
この0.100mol/L HClaq4.2mLが
混合溶液50.0mL中の添加された
NaHCO3に対応する。
・・・NaHCO3とHClは、下記のように
物質量比1:1で反応する。
NaHCO3+HCl→H2O+CO2+NaCl
物質量比1:1
よって混合溶液50.0mL中の添加された
NaHCO3の物質量50.0C2mmolと、
0.100mol/L HClaq 4.2mLの物質量は
等しい。
というわけで、下式を得る!

∴C2=8.4×10-3mol/L
Na2CO3のC3mol/Lの算出
先記のように、0.100mol/L HClaqが
第1段階の滴定でPPが変色する間で
加えたV1=22.1mLの
物質量と、混合溶液50.0mL中の
Na2CO3の
物質量50.0C3mmolとが
等しいのは明らかです!!
てなわけで、下式を得ます。

かなりたいへんでした。
書き上げるの。
なのでキッチリ復習してください笑

