この記事では濃度計算の
解法についてお話しして行きます。
この問題を解説して行きます。
まずは自力で確実に解いてください、
自分で考える事が大切です。
まだ解けていない人は、これ以上
下はまだ見ないでください。
もし、まだ合法カンニングペーパーの
使い方を知らない人は、
この記事で確認して置いてください。
それではこの問題を手順に沿って
解いて行きます。
[quads id=5]濃度変換の解法①合法カンニングペーパー
1つ目の解法は、
合法カンニングペーパーを使う
解法となります。
合法カンニングペーパーの基本は、
→単位を参考に分母と分子を別々に
変換する
ことです。
単位に置ける留意点
そして、大事なのが単位に
( )をつける事でした。
たとえば、g(質)なのかg(全)
なのかでは全く扱いが変わります。
今回の問題では
質量%が20.0のNaOHaq
(aq:aqua 水溶液を表す)
のモル濃度への変換なので、
このときは、
NaOHaq20.0%は、先ほどの記事の
通り、
20.0g(NaOH)/hg(全)
=20.0g(NaOH)/100g(全)
としましょう。
そして、
密度は、g(全)/cm(全)=g(全)/mL(全)と
分子、分母に(全)がつく事を
絶対に忘れないでください。
質量%→モル濃度への変換するときに
これを覚えておく事で
『脳みそを全く使わなくても
出来るようになります』
骨格作成
骨格を作成して行きます。
骨格は分子分母の単位を
『別々変換』するのでしたね。

分子はg(NaOH)をM=40.0g/molで割ってmol(NaOH)に!
分母はg(全)に密度の逆数mL(全)/g(全)を×とmL(全)に!
mL(全)を1000で割ってL(全)に!
このようにして代入して計算すると、
6.10mol/Lと言う答えになります。
濃度変換の解法②ズルい解法
濃度変換の解法の2つ目は、
上の記事でもお話ししました
公式に代入するだけです。
一切記述問題が無い、
私大入試や、センター試験、
などではかなり有効で、
早くて、ミスが少ないので
確実に覚えておいてソンはありません。
センターでは真面目に計算している
のはアホなので絶対にこの裏技を
覚えておいてください。
公式は下のもので、

俺は下を覚えていました。
解答は、
NaOHaqのモル濃度をCmol/Lと
して、
代入するだけ、
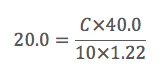
これをC=に変換すれば、
C≒6.10mol/L
となります。
これが濃度変換問題①の解法です。
普通に無料テキストや
俺の記事を読んでいた人は、
もうちょろくて余裕だったはずです。
キッチリ復習しておいてください。
ここまでの動画で復習しましょう!

