こんにちは。


炭酸水素ナトリウムは受験に頻出の超重要物質です。この記事ではその性質を徹底的に解説しますので、しっかり読んで要点を押さえておきましょう!
目次
炭酸水素ナトリウムの化学式・式量・用途
炭酸水素ナトリウム(NaHCO3)は、アルカリ金属であるナトリウムイオン(Na+)と炭酸水素イオン(HCO3–)が1:1の割合でイオン結合した炭酸水素塩です。
一般的には「重曹」または「ベーキングソーダ」という名前で知られています。
重曹は、炭酸水素ナトリウムの別名「重炭酸曹達」(漢字でソーダは曹達と書きます)の略です。

化学式(組成式)は、NaHCO3
式量は、84(イオン結晶なので「分子量」ではありません)
常温常圧では白色の固体です。

食塩水から安価で生成でき、人体への毒性も低いことから食品添加物や医薬品に広く用いられています。
炭酸水素ナトリウムの性質 何性? pHは?
すこし水に溶ける
ナトリウムイオン(Na+)と炭酸水素イオン(HCO3–)の周囲の水分子を引きつけ水和する力は同じくらいです。
そのため取り込んだ水和水の領域(水和殻)が無理なく重なり合い、結晶を作る作用が大きくなるため水への溶解度は 110g/l(30℃)とあまり大きくありません。
下のように電離し、少しだけ水に溶けます。
NaHCO3 → Na+ + HCO3–
水に溶けると弱塩基性を示す
炭酸酸水素イオンが加水分解して水酸化物イオンを生じることによりpH8.3程度の弱塩基性を示します。
HCO3– + H2O ⇄ H2CO3 + OH–

分解して二酸化炭素を生じる
炭酸水素ナトリウムは熱したり、酸を加えたりすると二酸化炭素を発生させます。
名前に入っている「水素」は発生しません。
パンケーキやカルメ焼きの生地に混ぜて加熱すると、発生する二酸化炭素が生地を膨らませます。

これは中学理科・高校化学の超重要反応ですので、次のセクションでいったいどのようなことが起きるのかをしっかり確認しておきましょう!
炭酸水素ナトリウムを加熱すると 〜熱分解反応〜
この記事の中で一番重要なのはココです!
炭酸水素ナトリウムを加熱すると、以下のように分解します。
2NaHCO3 → Na2CO3 + CO2 + H2O
発生するのは二酸化炭素と水、加熱後に残る白い粉末は炭酸ナトリウムです。ゴロ合わせでこう覚えましょう。
一生懸命バイオリン二重奏を演奏するなつこさんのショーツ(パンツ)が見えそうになったけど、俺は紳士だから目をそらして見なかったぜ。というイメージです。
しかし他のナトリウム化合物(塩化ナトリウムや炭酸ナトリウムなど)は熱を加えても融解するだけなのに、炭酸水素ナトリウムはなぜ分解するのでしょう?
それは炭酸水素イオン自身による中和反応のせいです。
炭酸水素イオンは下のような平衡状態になっています。
2HCO3ー ⇄ CO32ー + CO2 + H2O
加熱することで二酸化酸素が出て行くと、平衡が右にずれどんどん分解が進むのです。
炭酸水素ナトリウムを熱分解する実験は、下のような装置で行います。
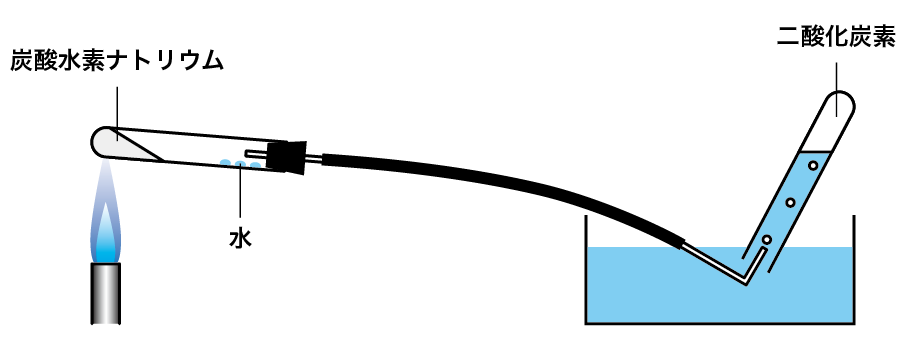
加熱する試験管の口を下げるのは、発生した水が加熱部分に触れて試験管が割れるのを防ぐため。
そして火を止める前に水上置換を行なっているガラス管を水からとり出すことが重要な操作です。
火を止めると、熱していた試験管の中の空気が冷やされて収縮します。
このときガラス管を水の中に残したままだと、水が吸い込まれて逆流し試験管の熱していた部分に触れ、割れてしまう可能性があります。
炭酸水素ナトリウムに塩酸を加えると 〜弱酸遊離反応〜
炭酸水素ナトリウムに塩酸を加えると、以下のように分解します。
NaHCO3 + HCl → NaCl + CO2 + H2O
キッチン実験でよく行われる酢酸(酢)との反応の場合はこうなります。
NaHCO3 + CH3COOH → CH3COONa + CO2 + H2O

炭酸(H2CO3)よりも強い酸と反応すると二酸化炭素と水が発生し、ナトリウム塩水溶液が残ります。
炭酸水素ナトリウムと炭酸ナトリウムの違い
炭酸水素ナトリウムを加熱した時に残る炭酸ナトリウムは、名前は似ているのですが性質は大きく異なります。
違いをまとめたのが下の表になります。
| 炭酸ナトリウム | 炭酸水素ナトリウム | |
| 別名 | 炭酸ソーダ | 重曹 |
| 水溶性 | 水によく溶ける | 水に少し溶ける |
| 塩基性 | 強い | 弱い |
| 風解性 | あり | なし |
| 熱反応性 | 熱しても分解しない | 熱すると分解して、炭酸ナトリウム・二酸化炭素・水を生じる |
性質の違いを利用して、炭酸水素ナトリウムの熱分解反応の前と後で異なる物質になっていることを確かめる実験がよく行われます。

反応前の炭酸水素ナトリウムは水に溶けにくく、水溶液も弱塩基性です。
しかし反応後に残った炭酸ナトリウムは水によく溶け、水溶液の塩基性は強くなります。
炭酸ナトリウムの性質についてより詳しく知りたい人は、ぜひこの記事を読んでみてください。
炭酸水素ナトリウムの製法
炭酸水素ナトリウムはアンモニアソーダ法、別名ソルベー法によって大量に生成されます。
まず食塩水にアンモニアを溶かします。
ここに二酸化炭素を通すと、炭酸水素ナトリウムが沈殿するのです。
NaCl + NH3 + H2O + CO2 → NaHCO3 + NH4Cl
反応はこれで終わりではなく、炭酸ナトリウムの製造まで行われます。
ソルベー法のより詳しい説明も、この記事を読んでみてください。
まとめ
この記事では超重要物質「炭酸水素ナトリウム」の性質を徹底解説しました。
炭酸水素ナトリウムの性質は
- 少し水に溶ける
- 水溶液は弱塩基性をしめす
- 分解して二酸化炭素を生じる
です。
また熱分解の化学反応式は
2NaHCO3 → Na2CO3 + CO2 + H2O
です。
















