昨日、こういう質問が来ました。
という問題の解答解説に対して、
なぜ、左辺のnについて、モル利用(49/22.4)を使えないのですか?
左辺のnの求め方について、使い分けがあるんですか?
ヘンリーの法則がわからない人のために、もっとざっくり質問内容は、
49mLの気体の体積がわかってんだったら、なんで22.4を使わず状態方程式で解いたのか?
っていう質問です。この疑問って思ったことある人が多いと思います。
体積を見たら全て22.4で割る習慣ができている人もいます。しかし、22.4L/molを使ってはいけない状況も実はかなりたくさんあるんです。
- 標準状態体積が22.4L/molであることの求め方と導出過程
- 導出過程から考えるに22.4L/molは意外と使えないという事実
本記事を読むことで、molを求めるときに体積を22.4で割るやり方は、意外と使えないことがわかるでしょう。
目次
標準状態体積22.4L°/molの求め方と導出過程
標準状態で1molあたりの体積なので、P=1.013×105Pa(=101.3kPa),n=1mol、R=8.31×103=8.31k、T=0℃=273K
この時の体積を求めればいいので、状態方程式に代入して、
.jpg)
ちなみに、このk(キロ)=103です。この使い方は補助単位の記事で学んでください。
キロを使うことで、キロ同士が相殺されます。よって

となります。よって標準状態の時の気体分子1molの体積は22.4Lとなります。


これは気体の種類関係なく、アボガドロの法則で、
「同温、同圧の時、同数の分子を含む場合気体の体積は同じである」
ことが示されているんだ。
なので分子の数が1mol=6.02×1023個の時は、同温同圧ならば、気体の体積は同じになります。
よって標準状態のとき気体の体積が44.8Lだったら、その気体の物質量は、
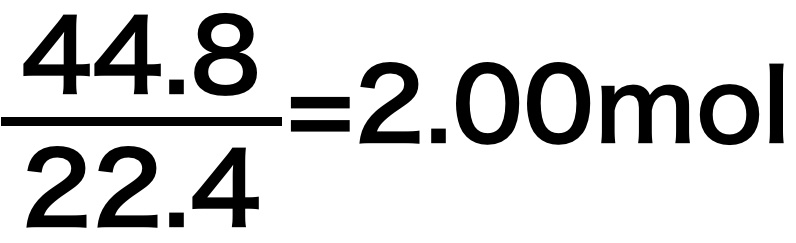
2.00molになります。
これは、確かに革命的に計算が楽になります。本来だったら、
(101.3k)(44.8)=n(8.31k)(273)
を解かなければならないのですから。大幅に計算の負担が減ります。
ただ、肝に命じて欲しいのが、これは標準状態のみ使えるのです。
だって導出するときに標準状態の数字を入れて22.4Lを導出していますよね。
なので気体の圧力が1.5×105Paの場合は使えないし、気体の温度がT=300Kの時も使えません。
冒頭の例題
このとき使えるんじゃね?って思いませんか?
ただこのとき「少し怖い」という感覚を持って欲しいのです。
1.0×105Pa、0℃で22.4L/molを使うのは危険である理由
1.013×105Paにおける1molの体積が22.4です。100kPaの時に使うと、、
答えは大きくは変わらないけど、少しは変わる
のです。先ほどの導出を101.3kPaではなく、100kPaにすると以下のようになります。

確かに、これで問題なくいける場合もありますが、若干答えの数字が模範解答と異なることがあります。こういう時に博打的に22.4を使う必要はないのではないか? と思います。
また化学の計算問題の観点でも話します。
この問題文を見てもらえればわかりますが、有効数字2桁です。

まとめ:22.4L°/molとの付き合い方
問題文に書かれていたら、そりゃあもう100%使えます。

って思うかもしれませんが、こういう問題の状態方程式は、RやPなどかなりの部分が約分されます。なので、意外と計算自体面倒じゃないことも多いのですよ。














