こんにちは。




原子半径という概念の理解は難しく無いのですが、同一周期で比較した場合に希ガスの原子半径が一番大きくなる理由をよく分かっていない人が多いようです。
しかもこれ、詳しく説明している教科書や参考書があんまり無いんですよね。
そこで今回は原子半径の謎について、トコトン解説していきます!
目次
原子半径とは?


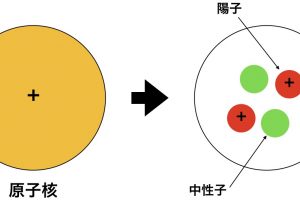
原子は中心にある正の電荷を持った原子核のまわりを、負の電荷を持った電子が飛び回っている構造をしています。
しかし電子は完全に自由に飛び回っているわけではなく、電子殻と呼ばれる軌道上に存在しているのです。
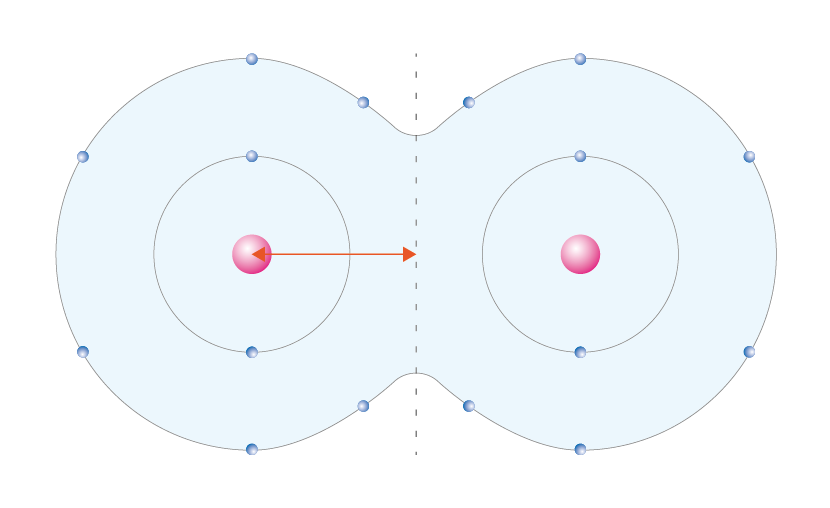
原子半径は原子核の中心から最も外側にある電子核(最外殻)までの距離です。

原子半径の基本的な法則は下の二つです。
- 同じ周期では原子番号が大きくなるほど、原子半径は小さくなる
- 同じ族では原子番号が大きくなるほど、原子半径は大きくなる
⬇︎つまり
周期表の左下に行くほど原子半径は大きくなり、右上に行くほど原子半径は小さくなる
※(後ほど説明しますが)この法則には例外があるので、注意が必要です。
原子半径は「同じ族」では原子番号が大きいほど大きい

周期表の周期は「電子がどの電子核に配置されるか」によって決められています。
第1周期はK殻に電子があるHとLi、第2周期はK殻とL殻に電子があるBe・B・C・N・O・F・Neという感じです。
つまり同じ族で比較すると原子番号が大きいほど、つまり周期表の下に行くほど多くの電子殻を持っていることになります。
電子が配置される電子殻が増えれば増えるほど、原子のサイズは大きくなっていくのです。
原子半径は「同じ周期」では原子番号が大きいほど小さい


例として、第二周期を見てみましょう。
第2周期の原子のK殻は電子で満たされて閉殻となっており、L殻が最外殻になっています。
このL殻の電子を中心に向かって引っ張って繋ぎ止めているのは、原子核の持つ正の電荷。
Liは3つある正の電荷のうち、K殻を引っ張る+2の電荷を除いた+1の電荷で最外殻電子を引っ張っています。
Beは+2の電荷で最外殻電子を引っ張り、Bは+3の電荷で最外殻電子を引っ張り…
という風に、原子番号が大きくなるほど最外殻を引っ張るのに使われる電荷が大きくなっていきますね!
そのため同一周期では原子番号が大きくなるほど、電子は中心に引き寄せられ原子半径がはどんどん小さくなるのです。

ちなみにこの「内側の電子殻に使われる電荷を差し引いた最外殻電子を引っ張る電荷」のことを有効殻電荷と言います。
とっても便利な表現なので、有効殻電荷について詳しく知りたい人はこの記事も読んでみてください。
希ガスの原子半径はなぜ大きい?
しかし上で述べた法則には、「例外」があります。
下のグラフを見てもらうと分かる通り、同一周期で原子半径が最大なのは「希ガス」なのです!
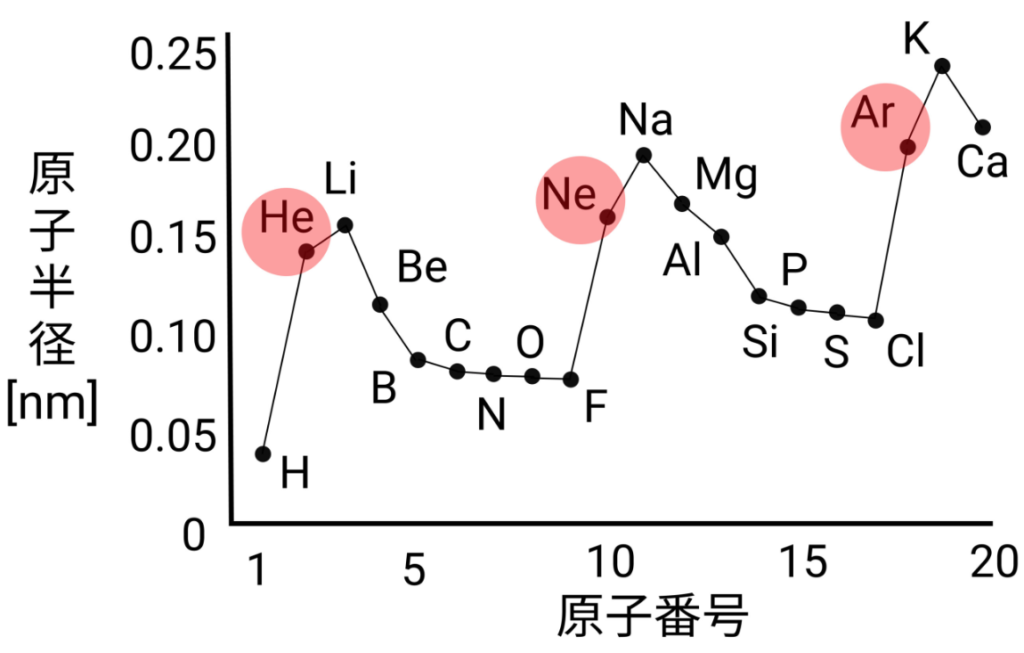


結論、希ガスの原子半径は「原子半径の定義のせいで大きくなっている」のです。
実は原子の半径を直接測定する方法はこの世に存在しません。

確かにそうですよね。
だって、最外殻とかの電子殻って別に目に見えるものではありませんから。
だから、原子半径は便宜的に別の方法で算出します。
なんですよ。
つまり原子半径は直接測れないので、X線回折などの方法でその原子が金属や結晶の状態のときの結合距離を求め、その半分を原子半径と考えるのです。
しかし、この方法を希ガスに用いることはできません。
よく思い出してください。
希ガスって「単原子分子」って言いましたよね!
結合しないので、結合距離を用いた計算によって「原子間距離」を求めることができないんですよ!
そこで希ガスの原子半径は、液体になった時の原子間距離=ファンデルワールス半径を用いています。
ファンデルワールス力とは、固体や液体の状態の原子・分子がお互いに引き合う力のこと。
原子や分子がファンデルワールス力によってお互いに接触したこの状態の核間距離を、ファンデルワールス半径といいます。
一方、共有結合や金属結合は最外殻の電子を共有するので核間距離、すなわち金属結合半径や共有結合半径はファンデルワールス半径よりも短くなるのです。

この原子半径の定義のバグによって、希ガスの原子半径は同一周期の他の原子に比べてなぜか大きくなってしまっているんですね。
まとめ
原子半径について、理解は深まりましたか?
今回のまとめは
- 同一周期では原子番号が大きくなるほど、有効核電荷が大きくなり原子半径は小さくなる。
- 同一族では電子番号が大きくなるほど、電子が配置される軌道が増えるので原子半径は大きくなる。
- 原子半径を直接計測する方法はない。
- 1族〜17族の原子は共有結合半径or金属結合半径(結合距離÷2)を原子半径として用いる。
- 18族の希ガスは化学結合しないので、ファンデルワールス半径を原子半径として用いる。
- 最外殻の電子を共有する共有結合半径や金属結合半径に比べて、原子が接しているだけのファンデルールス半径は大きくなる。
- そのため希ガスの原子半径が同一周期で最大になる。

です!
「なぜそうなるのか?」と疑問を持ち、その謎を明らかにして行くことが化学の力をつけるためにはとっても大切。
質問等があれば、コメント欄へどうぞ!