今日は、塾生から質問があった内容です。

です。確かに、この2つってすごく違いがわかりにくいんですよね。なんとなく違うことはわかるものの、、、
2年生から質問があったんですが、3年生は大丈夫ですよね?
『原子量は○○○で、質量数は○○』
だから2つの違いは、
『○○である!』
これの穴埋めが出来なかった人は、絶対に見てくださいね!
まず、最初に質量数と原子量のざっくりした定義の確認をします。とっとと本題の質量数と原子量の違いを見たい人は、そこまでワープできます。
目次
質量数とは?
質量数(しつりょうすう、mass number)は、原子核を構成する陽子と中性子の数を合わせたものを言う。 通常、Aで表す。 同じ原子番号であるが質量数(すなわち中性子数)が異なる原子は同位体である。
wikipediaから引用させてもらいました。

質量数=原子番号+中性子数
という公式は見た事が在ると思います。
でも、世の中には、同じ原子番号でも、異なる質量数の物が存在します。
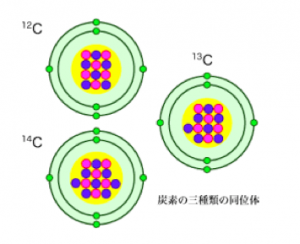
これらは、同じ原子番号の炭素でありながら、中性子数がことなることから、質量数が異なります。
つまり、質量数というのは、原子番号が同じでも、異なる事があります。
原子量とは?
一方原子量というのは、実は一定です。
炭素の原子量は12です。
13Cや14Cはもはや、この地球上にゴミ程度しかありません。
ほとんどは、12Cなのです。よって、原子量はもはや12なのです。
ここからがこのコンテンツの本番です。このまま読み進めてください!
原子量と質量数の違いは?
原子量と質量数は、同じになるものもあれば、異なる数値になることも多いですよね。これはなぜかというと、同位体があるからです。
質量数=原子番号+中性子数数です。同じ原子でも中性子の数が違うものを同位体と言います。原子量は同位体の質量数の期待値なのです。
どういうことかわかりやすくするために、高校生の年齢で例えますね。
まず、高校3年生というくくりがありますね。
高校3年生には、18歳の人もいれば、17歳の人もいます。ごく稀に19歳の留年している人もいます。ですが、8月くらいになると、高校3年生の平均年齢は、17.5歳になります。
高校3年生からランダムに一人選ぶと、17.5歳の期待値が得られます。実は原子量や質量数の世界も全く同じなんです。
高校3年生で17歳の人と18歳の人は同位体のようなものです。そして、ランダムに高校3年生から1人選ぶと、年齢の期待値は17.5歳です。
これを原子の世界に持ってくることができます。
同じ元素なのに、中性子の数の違いで異なる原子が存在します。35Clと37Clが存在したりします。この35と37は質量数です。
そして、自然界には35Clと37Clが存在するわけですが、自然界からランダムに塩素原子を取り出すと、35Clが手に入る確率が75%(存在確率)、37Clが25%です。
じゃあ、塩素を自然界からランダムに取るとした時、質量数の期待値は?
35.5ですよね(詳しくは次に演習問題で計算式も記しています)。この35.5が原子量なんです
- 質量数は、原子1つ1つの特徴
- 原子量は元素として見たとき、原子を1つ取り出したときに得られる質量数の期待値
では、演習問題でバッチリ頭にいれていきましょう。
塩素の存在比の問題を解いてスッキリさせよう!
天然の塩素には35Cl(質量数35.0)と37Cl(質量数37.0)の同位体が存在し、それぞれの存在比は75%と35%である。塩素の原子量を求めよ。
この問題の文章を読めば既にスッキリ頭の中でまとまったのではないでしょうか?
そう、35Clくん、37Clくん、もいるわけです。
そして、『高校3年生』というようなくくりのように、『塩素』というくくりで言うのが原子量です。
つまり、35Cl、37Clの平均値をだせばいいのです。
しかし、35Cl、37Clが等しく居るわけではなく35Clは75%で37Clが25%もいます。
存在比ですが、これは『確率』と考えるとわかりやすいです。つまり、35Cl、37Clがたくさんある箱から1個の塩素を取り出すと考えます。
このとき35Clを取り出す確率が75%なわけです。
つまり、原子量というのは、『期待値』なのです。
他にも期待の分野で、平均分子量を求める事が在ると思いますが、これは、すべて分子量の期待値なのです。
こう考えると、存在比から原子量を求めたり、平均分子量をもとめることなんて楽勝ですよね。
35×0.75+37×0.25=35.5
これがまさに期待値の求め方ですよね。
つまり、塩素が沢山在るなかから、塩素を取り出すという事象は、毎回質量数35.5の期待値があるということになります。
この期待値を『原子量』といいます。
まとめ
質量数=1人1人の個性(たかし、けんじ)
原子量=集団としての特徴(高校3年生)
存在比はそれを取り出す確率と考えると、『原子量』は期待値と言い換えられる。
結構整理できたんではないかと思います。それでは!