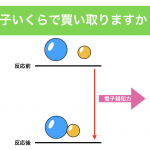
「イオン化エネルギーは陽イオンになりにくさ」「電子親和力は陰イオンのなりやすさ」こんな風に習いませんでしたか? はっきり言って、こんな習い方で2つを区別できるはずもありません。
というわけで、今日は全く新しいイオン化エネルギーの覚え方をお伝えしようと思います
- イオン化エネルギーをお金に例えて簡単にイオン化エネルギーの大小関係を理解できる方法。
- 電子親和力と混同することがなくなる覚え方
このイオン化エネルギーをお金に例えて覚えてしまうと、驚くほどスッキリ理解することができてしまうのです。また無理に言葉で覚える必要もなく電子親和力との違いもバッチリ理解できてしまいます。
これまでも、この例えをメルマガで1万人以上に教えてきましたが、多くの受験生がスッキリ理解できたと評判の覚え方です。

実際、これまでにサイトだけで100万人近い受験生に化学を教えて、今ではメルマガ読者だけで1万5000人に到達します。
目次
イオン化エネルギーとは?
原子が陽イオンになるのに必要なエネルギー

原子は原子核と電子からできていましたね。この原子核と電子の1個を分離する時に必要なエネルギーを第1イオン化エネルギーと言います。
てな訳で、お堅い説明はここまでにして、早速お金に例えて学んでいきますね。
イオン化エネルギーの大小はお金に例えたら楽勝です。

イオン化エネルギーはお金に例えたら、簡単に理解できます。
イオン化エネルギーとは、自分の電子の売値。いくらエネルギーと言うお金を貰えば、電子を手放してくれるか?
このように例えるとスッキリわかります。陽イオンになりやすいアルカリ金属なんかは、別にそれほどお金は必要ありません。

そもそもナトリウムの電子配置は、下のようになるので、電子を投げたほうが陽イオンとして閉殻構造を取れます。

なので、それほど電子を1個売るのにお金を受け取らないのです。Naの電子は安いのです。一方、ハロゲンの塩素は、

自分の電子が好きです。なぜなら、あと1個電子を受け取れば、閉殻構造を取れるからです。

電子をあと1個手に入れたら、アルゴンと同じ閉殻構造を取れるのに、わざわざ自分の電子を手放さなければならないのです。その時、自分の電子はめちゃくちゃ高く売りますよね。
塩素の電子は高額なのです。
イオン化エネルギーの大小を周期表で表すと?
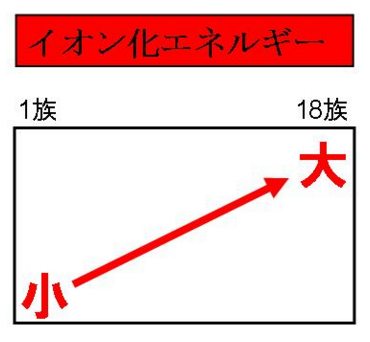
イオン化エネルギー 周期表
イオン化エネルギーは入試問題では、この周期表に絡めて出題されることが非常に多いです。イオン化エネルギーの周期表で表した特徴としては、右に行くほど大きく、上に行くほど大きいです。
なぜ周期表の右ほどイオン化エネルギーが大きい?
周期表の左の元素の原子は、電子を手放すことで閉殻構造になれます。だから自分の電子を高い値段をつける必要がないんです。つまり、周期表の左はイオン化エネルギーは小さいです。
しかし、周期表の右の元素の原子は、電子を手に入れることで閉殻構造に近づきます。てことは、本来電子を手に入れなければならないのに、自分の電子を手放している場合じゃないんですよ。
どうしても電子を売らなければならないっていうなら、その電子は超高額にしますよね。だから、周期表の右側ほどイオン化エネルギーは大きいのです。
なぜ周期表の上ほどイオンエネルギーが大きい?
アルカリ金属内で比較します。Li(リチウム)とK(カリウム)を比較します。すると、

リチウムの最外殻の電子は、原子核から距離が近いです。一方、リチウムに比べてカリウムは、
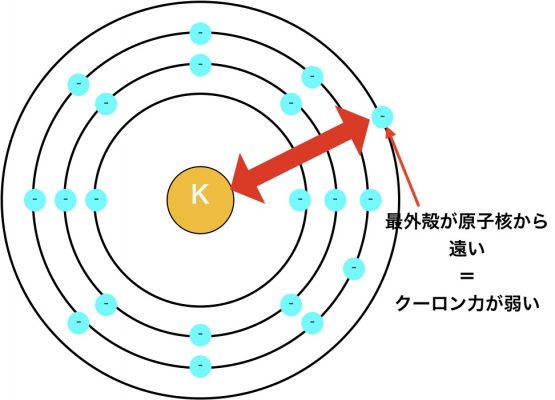
最外殻の電子が原子核から遠いです。
この原子核から電子が引きつけられる+とーの引力をクーロン力と言いまして、クーロン力は距離の2乗に反比例します。つまり、距離が遠いほど引き付ける力が弱くなります。
つまり、原子半径が小さい周期表の上の方は、原子核から電子がクーロン力で強く引っ張られているので、イオン化エネルギー(陽イオンにするために必要なエネルギー)は大きくなります。
一方、原子半径が大きい、周期表の下の方は、原子核が電子を引き付けるクーロン力が弱くなりますので、イオン化エネルギーは小さくなります。
イオン化エネルギーは、
- 同周期(周期表の横)は原子番号が大きいほど大きくなる(閉殻に近いのと有効核電荷が大きい)
- 同族(周期表の縦)は原子番号が大きいほど小さくなる(原子半径が大きく最外殻電子を引き付ける力が小さくなる)
受験勉強は努力だけでなくいい情報を仕入れることが重要です

受験勉強は、ただガムシャラに勉強をしていたらいいわけではありません。もちろん努力は必要ですが、今回のようにスッキリ理解できる「正しい知識」を手に入れないことには努力が報われません。
せっかく努力をするならば、効率よく努力をする必要があります。そのためには、正しい情報を手に入れる必要があります。
その点では、僕のメルマガはすでに1万5000人が読んでいますので、多くの受験生からの支持を得ている有益な情報と言えるでしょう。期間限定で無料電子書籍と無料動画講義をプレゼントしていますので、今のうちにメルマガ登録をしておいてください。