こんにちは。
脂肪族の勉強で、
なかなか重要なのが、
このアルコールです。
アルコールはちょっと反応
させるだけで、
アルデヒドになったり
アルケンになったりと
脂肪族の起点になっているような
物質です。

今日は、アルコールの脱水反応
をどのように構造決定に
活かして行くか、
それを学んで行きましょう。
目次
アルコールの脱水の触媒
アルコールってどういう
結合でしたか?
そう、σ結合でした!
σ結合はπ結合よりも
強固な結合です。
なので、この強固な結合を
切るためにはやはり
強い試薬を使わないとダメです。
ということで、
アルコールの脱水は、
強い試薬である、
濃硫酸を使います。
濃硫酸の脱水のメカニズム!
濃硫酸というのは、
98%以上の濃度の
硫酸水溶液の事です。
つまり、
98%H2SO4であり、
のこりたった、2%が水です。
そして
H2SO4って超強酸ですよね、
てことは、H+を
投げたくて投げたくて仕方が
ないわけです。

でも、
投げる相手が居ない、
希硫酸ならH2Oが豊富にあるので、
H2SO4から
H2Oめがけて、
H+を投げる事が出来ます。
H2O+H+→H3O+
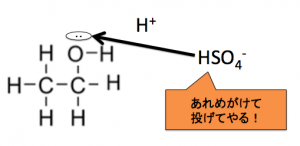
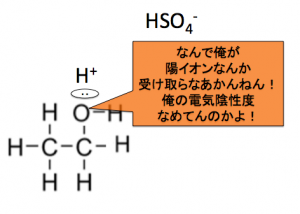
でも、濃硫酸が投げる相手が居ない、
よってアルコールとかを見ると、
-OHにむけてH+を
投げつけて、水が取れるようにします。
このメカニズムは、この後に
キッチリ説明してあります。
アルコールの脱水は2種類ある!
アルコールの脱水は2種類あり
その2つは温度で
区別されます。
分子間脱水
分子間脱水は
約130℃〜140℃で脱水すると、
起ります。
超詳しいメカニズムは次のように
なります。





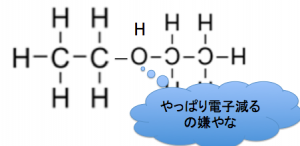
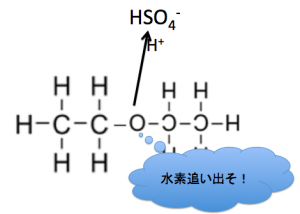
なので、130℃から140℃で
分子間脱水が起ると、
アルコールから『エーテル』が
出来ます。
分子内脱水
分子内脱水は
160℃〜170℃で起ります。





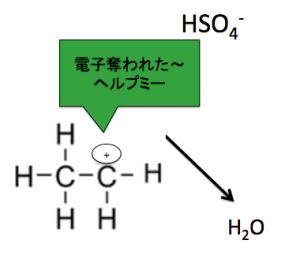
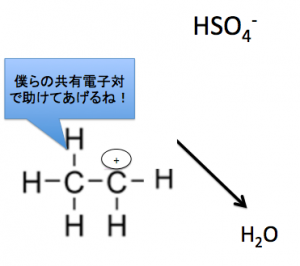

このように、約160〜170℃で
脱水を行うと、
アルコールからアルケンが出来ます。
ザイツェフ則
これは分子内脱水に関する、
経験則です。
アレクサンドル・ザイツェフっていう
おっさんが、発見したもので、
分子内脱水するとき、
たとえば、2-ブタノールとか、
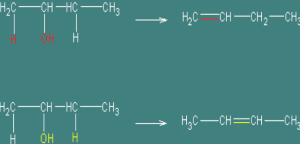
2種類できますよね。
このとき実は、
上が副生成物で
下が主生成物なんです。
ヒドロキシ基が脱水されるとき、
-OHの結合した両隣のC原子のうち、
水素原子の数の少ない方から
H原子が優先的に失われ、
それが主生成物となる!

だから、赤線で囲われた方、
が脱水する方が主生成物
であると言う事です。
似たような法則で
『マルコフニコフ則』というもの
があります。
マルコフニコフ則は、
水素化物が付加する時に
Hが多くついている方に
Hが付加するのでした。
つまり、
抜けるときは、ザイツェフ則!
というわけですね!
2つとも経験則ですし、
構造決定では時々、
知っている前提で問題が出る事も、
ありますし、
以前センター試験でも出てます!笑
なので、学校で習ってないから〜とか
ダメですよ〜
それではありがとうございました!















O原子がHイオンを受け取った後、水になっている反応は、
①O原子がHイオンを受け取って、OHーになる。
②硫酸の投げたHイオンと結びつく。
③水になる。
という解釈で合っていますか?
-OHのOに硫酸のHがくっつくことで既にH2Oになっています。
わかりました!
ありがとうございました。
脱水って二重結合でするのはわかるのですが、三重結合の時には起こらないのですか?
二重結合でも三重結合でもしません。
アルコールを濃硫酸なので脱水するとエステルを生じますか?
カルボン酸があれば。
何故濃硫酸の片方からしかhプラスは外れないんですか?
図解的にそう書いているだけで、そうとは限りません。