こんにちは。
幾何異性体を持つアルケンってシス型とトランス型で沸点や融点が違うんですよね。
なんで、アルケンはシス型の方が沸点が高いのでしょうか?
なんで、アルケンはトランス型の方が融点が高いのでしょうか?
実際にこのような問題が出てきます。なので、本記事ではこれらのアルケンの沸点と融点について解説していきます。
目次
有機物の沸点を決める要素
ここでの沸点に関しては、官能基をのぞきます。たとえば、カルボキシ基やヒドロキシ基があれば水素結合をしますので、チートで沸点が高くなります。

ここで比べるのは、ファンデルワールス力による沸点の影響です。
とはいえ、分子量の10000000000のものと分子量30の物を比べても相手になりません。
こちらにも書いていますが、ファンデルワールス力は分子量に依存します。
なので、今回の記事では、ある程度分子量が同じものでの戦いになります!
ファンデルワールス力を大きくするためには、、
ファンデルワールス力を大きくするには、『接触面積』を大きくする必要があります!
こちらにも在りますが、接触面積が大きくなればなるほど、沸点が大きくなります!
これを考慮して有機物の沸点を考えます。
アルカンの沸点は直鎖なのか?枝分かれなのか?
アルカンに関しての沸点の大きさの序列は下のような事が絡んできます。
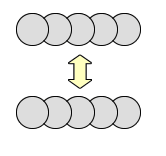

これだと上の方が接触面積が大きくなります。下の方が接触面積が小さくなりますよね!
つまり、アルカンの場合は、
枝分かれがない方が沸点が高い!直鎖が最強!ってことです!
アルケンの沸点の序列
次にアルケンです。ここでなにも考えていないとミスります!
アルケンも何も考えずに、『直鎖の方が良いんでしょ!』とかいっていると、陥ってしまいます!
しかし、そんな事はありません。
『接触面積が大きい』ほど『沸点が高い』のです。それが第1優先です!
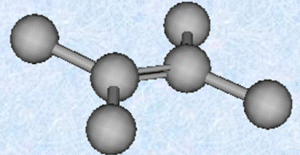
このようにアルケンは二重結合が在ると、『平面構造』になります!
一方、アルカンのように直鎖だけなら、どうなるでしょうか?
炭素というのは、実は、正四面体なんですよね。

このようになります。
だから繋がるとこのようになります。
だから、ブタンは下のようにぐるぐる立体的になり、ブタン分子同士が接触しにくくなっています。


下のブテンは、炭素骨格は平面上に全てのC原子がありますので、接触面積がアルカンの直鎖よりも大きくなります!
例題
それではこれらのことから次の物質でどちらが沸点が高いかを考えてみてください!

と

こいつらの勝負になります!
何も考えていないと下の方を選んでしまいそうです。なぜなら、直鎖だから。
しかし、そんな事は在りません。上の方が平面構造で、接触しやすいのです。
下は、直鎖の部分がすべて、正四面体構造なので、微妙に接触しにくいのです。
実際に見ると、2,3-ジメチルブテンの沸点は73℃ですが、1-ヘキセンは63℃ほどです。
平面構造が大きい方が、沸点が高くなっていますね!
このように、全て直鎖の方がいい!って言うわけではないんですよ!って事頭に入れといてください。
本質は、接触のしやすさですからね!















KINJITOでアルカンの沸点の見極め方は知っていましたが、アルケンはしりませんでした。この記事を読んでなかったらあやうく例題で下を選んでしまったでしょうね(笑
ありがとうございます!
すみません。伝えられていませんでした。
とにかく本質は『接触面積』だとわかれば勝ちです。
2,3-ジメチルブタンの沸点は57.9~58.3℃で、1-ヘキセンの沸点は63 °Cになっていますけど。
そりゃあ、アルカンだからね。
今言っているのは、2,3-ジメチルブテン。
なんかページバグってね
どこよ
分子同士の接触面積!なるほど!