ベンゼン環の構造式の書き方でなんか変なのありません?
普通ベンゼン環って書き方、

これですよね。
この構造式を書いていたら、なんか学校でちょっとイキってるやつで、下のベンゼン環を書きやがる輩が居ませんか?

みたいにちょっと上から目線で話してきます。

って疑問も湧いている人も多いでしょう。
今回はベンゼン環の真の姿に迫りながら、ベンゼン環というものを深掘りしていこうと思います。
ちなみに、受験化学コーチなかむらとしてインターネット上で受験化学を教えていますが、このベンゼン環の真の姿がわかった時に、大学入試試験の最重要問題構造決定が圧倒的に解きやすくなります。
どんなことがあっても理解するように努めてください。
目次
ベンゼン環の真の姿

ベンゼン環には実は構造式が2つあります。
あなたはベンゼン環は
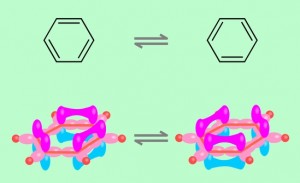
このように二重結合の位置が
移り変わると教わりましたか?
まあ高校化学ではそのようにごまかして教わります。
ちなみに、二重結合はσ結合とπ結合でできているのです。よく二重結合のことをこのように習うことがあります。

しかし、本来の二重結合は、

このように普通の化学結合の時
なので、ほんまもんの姿をお話しする事が出来ます。
ベンゼン環のほんまもんの姿っていうのは、実はこういう状態なんです

みんな繋がって雲みたいになっています。
これは、C-Cの間の結合がσ結合でその上にある雲のような結合がπ結合です。

二重結合はこのような構造になっています。上が二重結合の2本目の結合(画像では3箇所で結合しているように見えますが、π結合は上下で1本の結合と考えます。)です。
そして、ベンゼン環は6個の炭素原子の全ての上でπ結合をしているようなイメージです。
実はこれではないんです。これじゃなくてですね、ベンゼン環の場合は、
π電子が雲のように一周する
みんなが繋がっているのです。
そして、
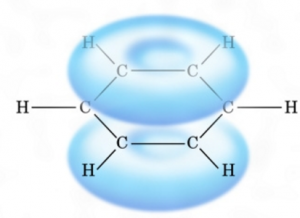
このようになります。
このようになることを非局在化と言います。
そして、非局在化しているこの状態を、共鳴状態と言います。
ベンゼン環の2つの構造式
ベンゼン環には構造式が2つあります。

この2つですが、この共鳴している状態を表して、6角形の中に、◯を書いているのです。
これが電子の雲を表しているのが、この◯です。
つまり粋ってたやつが使っていた、

この構造式ですが、実は本当に正しいベンゼン環の姿だったのです。
ベンゼン環は本当は二重結合と単結合の混在? それとも1.5重結合?

この構造式(ロビンソンの構造式)
と

この構造式(ケクレの構造式)
どちらが本質的なのか?というのを
考えて行きましょう。
ケクレの構造式は、
ベンゼンは、分子内に二重結合が
3つあるという考え方です。

ロビンソンの構造式は、
全体的に、1.5重結合のような
物が広がっていると考えています。
ベンゼンに水素を付加させて、
シクロヘキサンにするモデルを
考えます。
すると二重結合に水素を
付加させるときに発する
熱量は、およそ120kJ/molです。
なので、
このようなエネルギー図に
なるはずですよね。

なのであわせて360kJ程度に
なるべきですよね。
しかし、
実際に、ベンゼン環へ、
水素を付加していくと、
なんと、その熱量は、
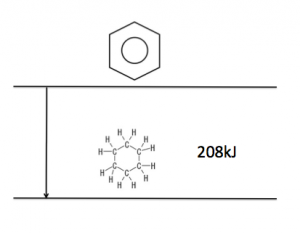
約210kJなんですよ!
てことは、
150kJどこいったの?
ってなるわけです。
どこいったんでしょうか?
それは、
共鳴する事により、
安定化するのです。

つまり、ベンゼン環は、共鳴する事によってやや安定化しているのです。
つまり、こちらの構造式の方が本質的と言えます。

入試ではどっちの構造式を使えば良いの?

では、悩みはこうなりますね、
どっちつかえばええねん!!
となります。
なので、今日はその明確な、決め方をお教えします。
それは、
『記入例に従う』
です。
構造決定の問題にはしばしば記入例が与えられています。
この記入例に従う事です。
ですが、ほとんどの場合、

で与えられます。
もし、記入例が無い場合は、必ず↓の構造式を書いてください。

受験では調子に乗らないことが重要です。
あんまり変な事はしないようにしましょう。
ですが、以前九州大学で、ロビンソン構造式でベンゼン環が与えられた事があります。

またさきほどの、エネルギー図の問題も九州大学で出た事があります。
今後の主流になる可能性もなきにしもあらず、なので、もしかしたらロビンソン構造式で与えられる事もあるかもです。
なので、とにかく記入例に従う事を心がけておいてください。
芳香族の計算のために覚えておくべき数字
このベンゼン環を含む
有機化合物の事を、
芳香族と言います。
芳香族化合物で計算する上で、非常に重要な数字があります。
それが、ベンゼン環の分子量です。
ベンゼン環の分子量は78です。
12×6+1×6=78
の78です。
これは覚えておいた方がいいですね。
こうすると、アニリンの分子量は?ときかれたら速攻で答えられます!
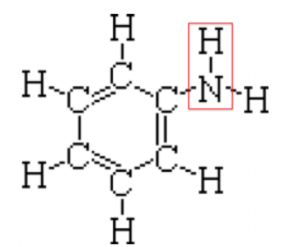
アニリンって言うのは、ベンゼン環に、赤枠で囲った、NHを足した物と言えます。
なので、78+14(N)+1(H)=93です。
また、逆に、『分子量93の芳香族の物質』という文言があれば、
とりあえず芳香族だから、93-78=15だなと考えます。

と考えます。
「だからアニリンだなと逆算する事が出来ます」

もし、92なら
「まず92-78しよう!すると、14だな!」
とわかります。
「てことは、CH2だな」
となり、
トルエンだとわかります。
このように、ベンゼン=78は非常に覚えておく恩恵が大きいので、覚えておいてください。

ベンゼン環ナハナハ(78)とおぼえてしまってくださいね!
まとめ
ベンゼン環は、

コチラの方が、より本質ですが、
テストでは基本的に、
コチラを書きましょう。
そして、
基本的に記入例に従いましょう!
さいごに、
ベンゼン環の分子量を覚えましょう!!















分子量94の芳香族は、フェノールではないでしょうか?94-78=16 16はO
CH2 は14です。トルエンの分子量は14+78=92です。
ありがとうございます。修正いたしました。
ナフタレンやアントラセンも同じ雲のようなものに挟まれた状態ですか?
そうですね!
例えば分子式がC7H8Oの時
クレゾールの構造式を書こうと思った時、
ベンゼンの分子式はC6H6ですよね?
Cがあと一つ、Hが二つ、Oが一つしか残っていないのに書けるのはどうしてですか?
置換反応ですね。置き換わると思ってください。とりあえずHの場所がフェノールとメチル基に入れ替わると思ってください。
× フェノール
○ ヒドロキシ基
ベンゼンC6H6のうち、H1つはCH3に置き換わり、さらにH1つがOHになるのですよね。2つのHが入れ替わるので、C6H6からH2を引いた、C6H4
にOHとCH3が足されると考えればよろしいのかと。