こんにちは。
芳香族のカルボン酸について学んで行こうと思います。
脂肪族のカルボン酸と芳香族のカルボン酸ではどのような違いがでるか?を説明していきます。
目次
芳香族カルボン酸と脂肪族カルボン酸の違い
芳香族カルボン酸と脂肪族カルボン酸は実は
ほとんど同じです。。
反応
まず脂肪族カルボン酸の反応ですが、
こちらにもかきましたが、
分子間脱水
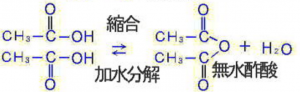
エステル化
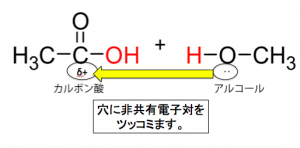
という反応でしたが、
カルボン酸も同様の反応をします。
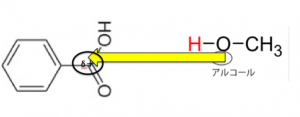
このように、セッ◯ス反応をして、電子を吸い上げられているカルボキシ基のカルボニル基に非共有電子対が突っ込みます。
この反応は何も変わりません。
性質
芳香族カルボン酸ももちろん普通に酸性物質です。
ただ、若干違うのが、芳香族カルボン酸は、ベンゼン環がある分、分子量が大きいです。
ベンゼン環がある時点で分子量が78分あります。
分子量が大きくなると、ファンデルワールス力が大きくなります。
ファンデルワールス力が大きくなると、沸点、融点が高くなります。
代表的な芳香族カルボン酸として最も有名な安息香酸がありますが、

安息香酸は、常温で下のような姿をしています。

安息香酸
先ほども触れたけど、
芳香族で一番単純なカルボン酸、
(もはやベンゼンにカルボキシ基ついてるだけ)

こいつです。
安息香酸は分子量が大きい事に加えて、分子間水素結合が出来るため、

沸点融点が高いです。
安息香酸の製法
この安息香酸を生成する方法があります。
実は、安息香酸は一発で安息香酸をつくりだすことができません。
なので、トルエンや、アルキルベンゼンを酸化する事で、作り出します。
(※アルキルベンゼンとは芳香族にアルキル基がついている物です。)
アルキル基というのは、アルカンからHを一個抜いた物です。
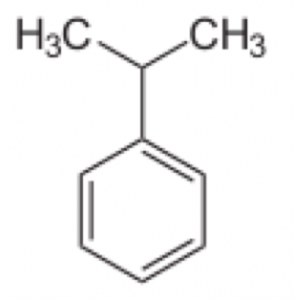
このアルキルベンゼンというのは、ベンゼン環に直接ベンゼン環に炭素がくっついているものです。
これを酸化すると、安息香酸になります。
そのメカニズムはこうです。

このようにアルキルベンゼン(今回は、キシレン)というのは、

このようにベンゼン環の共鳴の電子に包み込まれて、二重結合っぽくなります。

すると、KMnO4を酸性条件で使うと、酸化開裂が起りましたよね!これによって、安息香酸が出来ます。
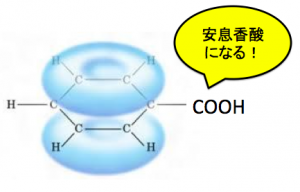
このようにして、安息香酸は生成されます。
このように芳香族のカルボン酸といえどほとんど同じです。対して変わりません。このように芳香族の勉強は、脂肪族が出来ていれば、かなりの部分はまかなえます。なので、基本は脂肪族です。
そして、きっちり脂肪族の内容を理解するには、理論化学や、化学基礎の知識がないとただの丸暗記になります。
以上です。最後までご覧いただきありがとうございました。














安息香酸はふつうのベンゼンよりもニトロ化などの反応が起こりにくいと習ったのですがその理由を教えていただけませんか?
メタ配向性のところで学べます。
オルトパラ配向性とメタ配向性の理由と見分け方大全!
上についてじぶんなりの解釈だと、陽イオンであるニトロ基は電子密度が高いところがすきだけど、安息香酸は電子吸引性のCOOHによってベンゼン環の電子密度がさがっているためベンゼンよりも反応しずらい、というのはまちがっていますか?
その解釈あってます