こんにちは。
アミノ酸は入試でも非常によく出て、天然高分子で一番良く出る内容です。
アミノ酸が重合するとタンパク質になり、私たちの生活にも深く関わってくるので興味を持てるのではないかと思います。
この記事ではα-アミノ酸の基本的なところとα-アミノ酸の覚えるべき構造、そしてその覚え方を解説していきます。
目次
α-アミノ酸とは
アミノ基を持つカルボン酸を『アミノ酸』と言います。他にも、ヒドロキシ基を持つカルボン酸を『ヒドロキシ酸』と言います。
これはカルボン酸の一種の分類方法であると以前説明しました。
そして、なぜα-アミノ酸と言うのかというと、αは炭素の位置を表すからです。
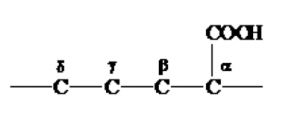
このようにカルボキシ基の隣の炭素から順番にα,β,γ,δ,と番号を振っていきます。
そして、アミノ基がα位に付くものをα-アミノ酸と言います。
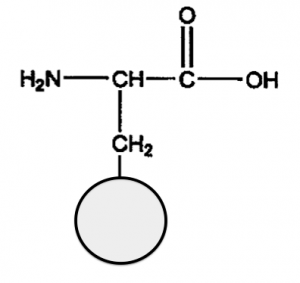
α-アミノ酸の超基本形アラニン
α-アミノ酸がこの構造であることには、実は深い意味があります。
そして、別の記事(アミノ酸の分子量の覚え方の記事)の所でも言いましたが、α-アミノ酸の基本形は、『アラニン』です。
なぜならアラニンが基本となり、アラニンの下に様々な官能基を付け加えて、それぞれのアミノ酸のオリジナリティを出していくからです。
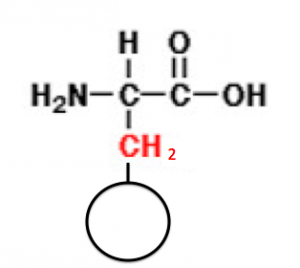
なぜ、このようにほとんど全てのαアミノ酸には、メチレン基(-CH2-)を挿入してあるのか?というと、
α-アミノ酸が重合して、タンパク質になったときに、

このようにタンパク質の骨格ができます。

このとき官能基が直接α位の炭素にぶら下がっていたら、骨格に官能基の影響を及ぼしてしまいます。
なので、メチレン基を挟む事で、その影響を和らげる事が出来ます。
α-アミノ酸の構造をアホみたいな語呂で覚えてみた
アミノ酸の勉強するときに非常に悩むのが、
「構造って覚えなあかんの?」って言う疑問です。
ちなみに分子量は覚えた方が良いと言う話をしました。
『α-アミノ酸の分子量は覚えるべきなのか?覚え方は?』
そして、構造を覚えるべきか?
この疑問に対する答えは、
「人それぞれ」
としか言いようが無いわけです。
なぜなら、「構造を書け」と聞いてくる大学もあるし、与えられている大学も在る。
だから、一概に、全員覚えろ!と言うわけではないし、これは自分の出願する大学の過去問を見てほしい。
その過去問のなかで構造を問われているかどうか?と言うのを確認してほしい。
ただし、構造がわかっている方が、アミノ酸の性質がわかりやすいです。またそれぞれのアミノ酸分子の特徴は詳細な構造が書けなくても覚えておく必要があります。
なので、今回それらをまとめていきます。
中性アミノ酸
中性アミノ酸とは、中性物質とかそういう事ではなく、モノアミノモノカルボン酸であるということです。
だから等電点もpH=6.0で微妙に酸性よりだったりする。厳密に中性な物質かというと、それは微妙。
グリシン
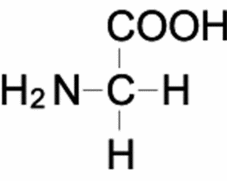
基本は、アラニンです。
グリシンはギリシャ語で『甘い』を意味しています。
グリシンの特徴は、α-アミノ酸で唯一不斉炭素原子がありません。
アラニン

さきほどいいましたが、このアラニンがα-アミノ酸の基本構造です。
分子量もアラニンの89から考えていきます。
次のバリン、ロイシン、イソロイシンは一括りでセットで覚えてください。
なぜなら、これらは、BCAAという分枝状アミノ酸に分類され、筋肉の生成に役に立つアミノ酸として性質が似通っています。
化学反応的にも、官能基がありませんので、同じような反応をします。
なので、リズム良く
『バリン!ロイシン!イソロイシン!』
と唱えまくろう!!
意外とこの順番が大事です。
バリン

バリンも化学的性質をもつ官能基を持つので、特に化学反応に関わる性質があるわけではない。
このバリンの覚え方は語呂があります。バリンの構造は『大』の字です。なので、これを利用します。
バリ島(バリン)大きい(構造)いいな(M=117)
これを用いる事で、バリンの構造を覚えられるだけではなく、分子量も覚える事が出来ます。
ロイシン
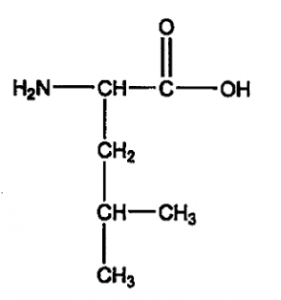
バリンにメチル基を挿入したもの。
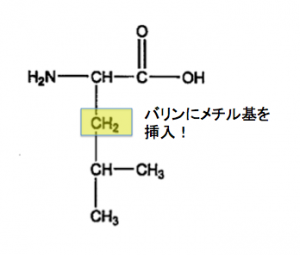
イソロイシン

このイソはisomerのisoからきています。isomerは異性体と言う意味ですので、ロイシンの異性体です。
メチル基の位置が1つ上に移動しています。
よってロイシンと分子式が同じであるため、分子量が同じです。
ロイシンとイソロイシンだけ分子量が同じで異彩(M=131)を放っています。
次のセリンとトレオニンは側鎖にヒドロキシ基が存在しています。
セリン
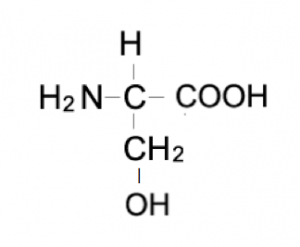
これは側鎖に親水性のヒドロキシ基がある事が特徴です。
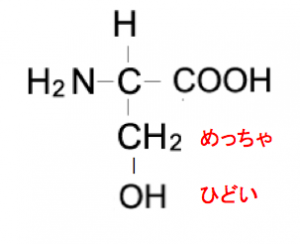
この構造の覚え方は、主鎖から、側鎖がメチル基、ヒドロキシ基なので、
芹菜(セリン)めっちゃ(-CH2-)ひどい(OH)いいとこ(M=10 5)なし
と言う風に覚えます。このごろはアミノ酸の分子量の記事で意味を確認してください。
トレオニン
これはあまりでないので、僕は構造は覚えていませんでした。
ヒドロキシ基がセリンと同様にあります。
フェニルアラニン

アラニンにフェニル基が付いているからフェニルアラニンです。
アラニンにフェニル基がついているからフェニルアラニンと言います。
これがわかっていれば、構造式も書けると思います。
チロシン
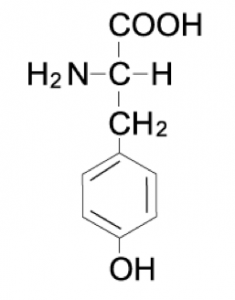
チロシンはフェニルアラニンにヒドロキシ基が付いたバージョンです。
チロシン祝い(181)
と勢いでフレーズで覚えてしまうんでしたね!
注意点は、チロシンはベンゼン環にヒドロキシ基がついたフェノール性物質なので酸性物質なのですが、『酸性アミノ酸』ではないのです。
そう、あの『酸性塩なのに酸性じゃない!』というようなもどかしい気持ちをもう一度味わう事になります。
酸性塩の定義は後で話しますが、『モノアミノ、ジカルボン酸』のことです。液性が酸性であろうと、カルボキシ基が1個ならば、酸性アミノ酸ではありません。
トリプトファン

側鎖に疎水性のベンゼン環があります。濃HNO3と反応させるとニトロ化により黄色になります。
また、塩基性にすると橙色になります。これをキサントプロテイン反応と言います。
以下は硫黄を含むα-アミノ酸です。
これらのアミノ酸を含むタンパク質に固体のNaOHを加熱して、酢酸で中和後、酢酸鉛(II)水溶液を加えると、黒色の硫化鉛(II)PbSの沈殿を生成する。
システイン
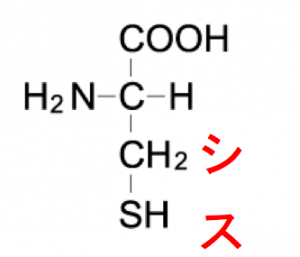
このようにシステインは硫黄を含まれます。
システイン側鎖のSHは酸化され、-S-S-のジスルフィド結合により分子間に架橋します。
これは、タンパク質の高次構造で使われます。
システインの分子量は、121です。特に語呂は無いですが、
システインイレブンスクエア(11の2乗=121)
という勢いで覚えてください。
メチオニン
メチオニン
塩基性アミノ酸
塩基性アミノ酸は、側鎖にアミノ基を持つリジン、アルギニン、ヒスチジンなどが塩基性アミノ酸です。
塩基性アミノ酸はジアミノモノカルボン酸(アミノ基×2でカルボキシ基×1)です。
等電点は、塩基性よりになります。
リシン
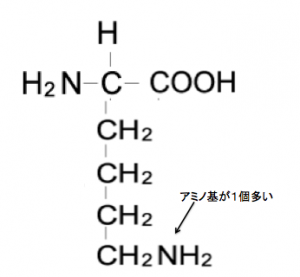
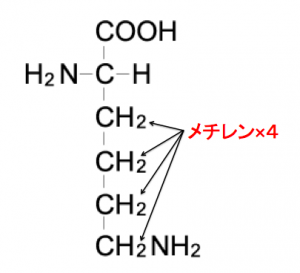
立身(リシン)出世して飯(メチル×4)余る(アミノ)色白(M=146)
アルギニン
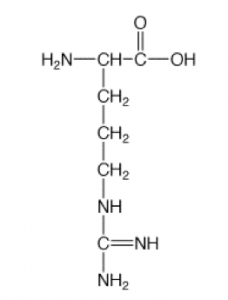
酸性アミノ酸
酸性アミノ酸の定義は、モノアミノジカルボン酸です。
側鎖に酸性を示すカルボキシ基がある、アスパラギン酸やグルタミン酸がこの酸性アミノ酸です。
酸性アミノ酸は等電点が、酸性によります。
アスパラギン酸

アスパラギン酸めっちゃ(メチレン)軽い(カルボキシ基)
って構造を覚えてください。
グルタミン酸

グルタミン酸は、味の素の原料となります。
グルタミン酸美味しいな(M=147)
いかがでしたか?
なかなか沢山ありますが、語呂で覚えてみてください!
自分で作る方がもちろん、良いですが、そんな時間が無いのでこの記事の語呂を参考にしてみてください!














アミノ酸、途方に暮れていました。
ありがとうございました。(´;ω;`)
いえいえ、ここからどんどん加速させて行きますよ!
システインの語呂を考えてみたのですが、
「めちゃスーハー、シスターの十二単(121)」
というのはどうでしょうか?
合成高分子についての記事が増えたら嬉しいです
トリプトファンのキサントプロテイン反応のところ、絵塩基性になってますよ。
とても分かりやすくていつも助かっています。
ありがとうございます!