中和滴定って元となる基礎がそれほど難しくないのに、入試問題になるとなんかすごく難しくないですか?実は中和滴定は、色々パターンがあって、この『逆滴定』がそう思わせているのです。
なので、この記事では、徹底的に!超丁寧に!『逆滴定』の解法をまとめていきます!
目次
逆滴定って何ですか?
多くの受験生は、この逆滴定をキッチリ順序立てて理解できていませんし、学校の先生や参考書、また他のサイトでも逆滴定をする理由を全く理解していない人が教えていることが多くあるのです。
あなたが知っている普通の『中和滴定』と『逆滴定』では、明確に違いがあります。その理解していないと、死んでも解けないのがこの逆滴定です。
しかも、案外出ますしね!なので絶対に出来るようにしてください。
まず、普通の中和滴定って、『濃度がわかっている酸または塩基』で『濃度または量がわからない塩基または酸』をポタポタ垂らしていって、濃度とか量を求めるものです。
普通の中和滴定って、この測定する物が溶液ですよね!しかし、今回の逆滴定は、測定する物が『水に溶けていないもの』なんですよ。
水に溶けにくいものだと、そもそも『濃度という概念がねえやん!』ってことなんです。
これが、自体を大幅にややこしくしているんです。
だって、濃度がわかっていたり、その溶液の中にどれくらいの酸があるのか?っていうのが決まっているから滴定して求められるんです。
だから、難溶性の酸塩基とか、気体とかでこの回りくどい逆滴定ってやつをやらないといけないのです。いい迷惑だ、、
とはいえ、結局入試で出るのは、まず気体だと思って大丈夫です!
普通の中和滴定は、

この図のようにわからない量を求めるために普通に滴定すれば、1対1対応で量がわかるようになったのです。
つまり、酸の溶液を知りたければ塩基で一回滴定したらすぐに反応がわかったのです。そう、溶液を滴定することは簡単なのです。
しかし、気体の量を知りたいとなれば、話は別です。なぜなら気体を滴定することができないからです。

例えば、この二酸化炭素のモルを知りたいとします。てことは、まず溶液に溶かす必要がありますよね。
しかし、この二酸化炭素をすべて水に溶かしきることは出来るでしょうか?

水だと100%溶かし切ることはできません。
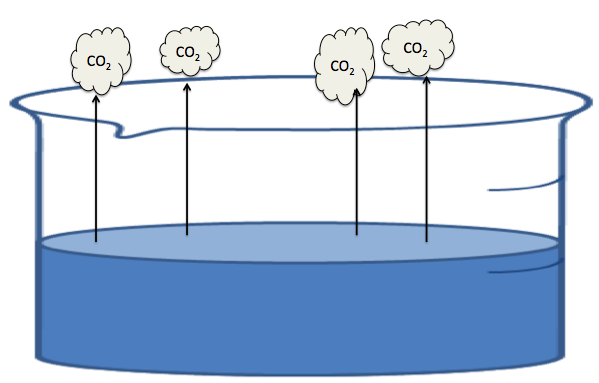
このように、溶けきれなかった気体が一部出てきてしまいます。
そこで、水ではなく二酸化炭素のように酸性の気体は、強塩基で中和してしまって塩として溶液中に閉じ込めておくのです。

このように水酸化ナトリウムや水酸化バリウムなどのような強塩基を使えば、二酸化炭素と中和反応をしてNa2CO3やBaCO3として溶液中にとどめておくことができます。
すると、外に出ていく気体をなくすことができます!このとき重要なことは、水酸化ナトリウムや水酸化バリウムは多めに準備しておくということです。
水酸化ナトリウムを多めに用意して置かなかったら、二酸化炭素を中和しきれずに二酸化炭素が気体に戻ってしまうからです。

このようになるのです。(後ほど二酸化炭素の逆滴定については徹底的に解説します)で、この気体の量をそうやって求めるかって言うと、

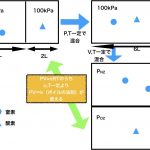
このように、黄色矢印の部分を求めることができれば、全体から引けばわからん気体の量がわかります。このように引き算で求めるのです。
これがざっくりとした逆滴定です。
それでは、次の章から入試で出題される2つのパターンについて考えていきましょう!
逆滴定で調べる4パターン
逆滴定で出題される問題は4パターンです。この4パターンさえマスターしたら必ず解けます。そして4パターンのうち3パターンは全然難しくないです。
しかし、一つのパターンは、かなり難しいです。まず、この記事だけで全て解説するのはあまりにも難しいので別の記事にも渡って解説します。
まず逆滴定を4つに分類するとこうなります。
| 気体 | 過剰溶液 | 滴定溶液 |
| アンモニア | HCl | NaOH |
| 二酸化炭素 | BaOH | HCl |
| 二酸化炭素 | NaOH | HCl(ウィンクラー法) |
| 二酸化炭素 | NaOH | HCl(ワルダー法) |
このような分類になるわけですよ。
普通二酸化炭素の逆滴定は水酸化バリウムを使うと楽に出来ます。なぜならBa2CO3として沈殿するからです。しかしNaOHを使う問題もよく出ます。むしろ難関大はNaOHを使うパターンの方がよく出ます。
これを使うと二段滴定が混ざってきて問題を難しくすることが出来るからです!では、まずはこの記事では、アンモニアと二酸化炭素の逆滴定を見ていきましょう!
アンモニアの逆滴定
アンモニアを中和滴定で定量したい、じゃあ、アンモニアを水に溶かそう!と思いますが、冒頭でも話しました。気体を水に完璧に溶かすのは至難の業です。
どれだけアンモニアが溶けやすいと言えどもすべて解けきるのはむずい。
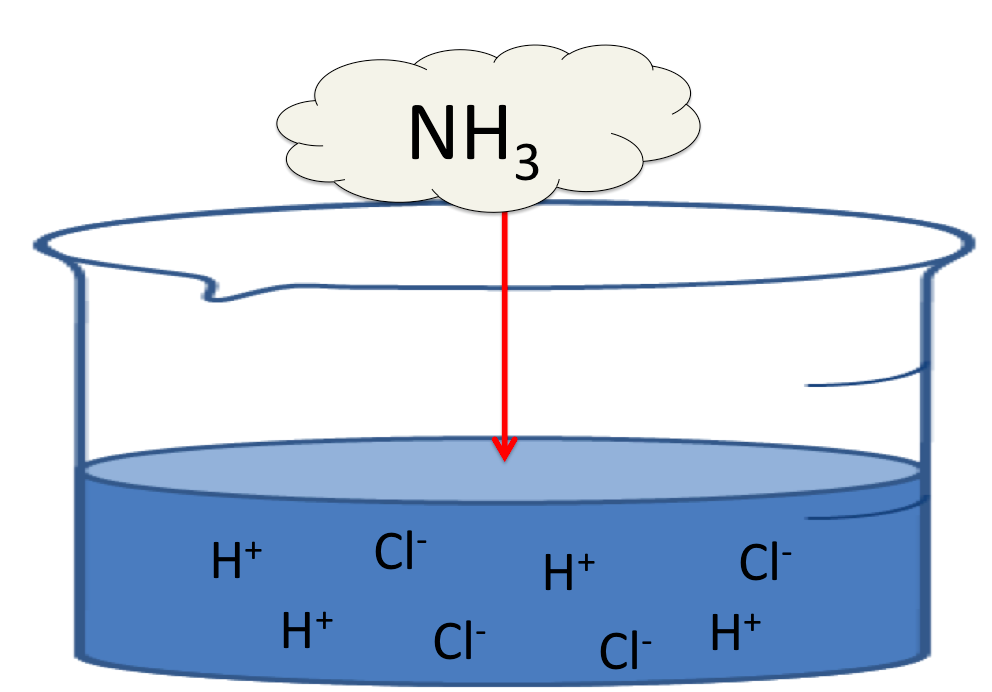
全て溶けないと中和滴定でNH3の量を測ったとして、それは元の量じゃない、ということは、正確にもとの量を測る事が出来ないのです。
つまり、先程行ったようにアンモニアを『強酸』で中和して溶液中にとどめておきます!
NH3の逆滴定の手順と物質量の関係
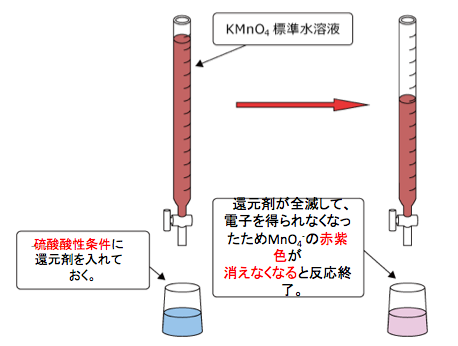
水にNH3は完全には溶けないので、大量の塩酸の標準溶液(濃度がわかっている溶液)に中和吸収させるのです。

塩になることで溶液中に確実に溶けて、空気中に出ていくことがあらへん!ここで中和で100%NH3を溶液中にとどめておきます!
過剰でないとアンモニアを全て中和吸収できるか微妙になってしまいます。だから、明らかに多い量のHClを用いるのです。
このときの反応式はNH3+HCl→NH4Cl ⇒NH3の物質量は、下の線分図より下式の用に求められる。
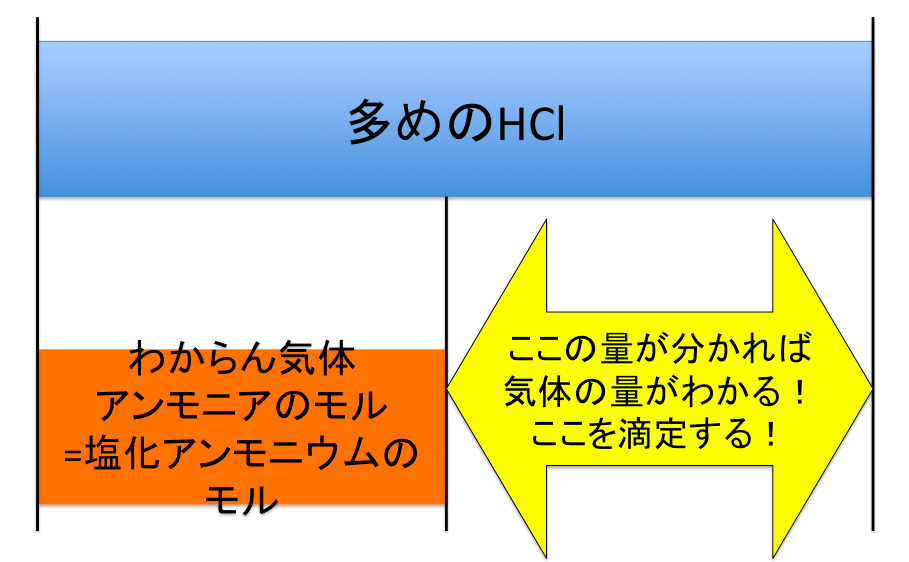
そして、上の図の

この黄色矢印の部分をNaOHで滴定してどれくらいのモルかわかれば、必然的にNH3のモルがわかります。

まあ、ここまで余裕で理解したって人は、もう後は早い。もうチェック・メイトしてる。
NH3の逆滴定の滴定曲線とpH指示薬
そう、中和滴定といえば滴定曲線。この滴定曲線のことも考えていきましょう!
実は、この逆滴定って
逆滴定の手順
①NaOHとHClの中和(⇔の部分)
②NaOHとNH4Clの弱塩基遊離反応
のように二段階になっています。
先程は、二酸化炭素のモルだけに注目したのですが、HCl VS NaOHの中和が終わった後もNaOHを滴定し続けると、NaOH VS NH4Clの弱塩基遊離反応が起こります。
pH指示薬
NH3の逆滴定では、終点を知るpH指示薬にメチルオレンジ(MO)かメチルレッド(MR)を用います。
その理由は、NH4Clがあるため、塩の加水分解をして溶液の液性が酸性になるからです。
最初溶液の中には
HCl+NH4Clがあります
そして、その後NaOHを滴下すると、HClとNaOHの中和が行われます。この中和が終了したときの中和点がNH4Clの塩の加水分解の影響で酸性になるから酸性領域に変色域を持つメチルオレンジかメチルレッドを使います。
pH指示薬選択の理由
このHClaqがNH3を中和吸収した溶液は
過剰のHClと中和で生じた
NH4Clの
HCl+NH4Cl混合溶液となっている。
この溶液をNaOHaqで滴定した滴定曲線の
概形を考えて行きます。
HCl+NH4Cl混合溶液をNaOHaqで
滴定した場合、下記の①〜③の順に反応が起きます。
HCl+NaOH→NaCl+H2O②溶液中のHClの中和反応が完了後、NH4ClがNaOHと弱塩基遊離反応する。
NH4Cl+NaOH→NH3+H2O+NaCl
弱塩基のアンモニアが
強塩基の水酸化ナトリウムに
追い出される反応③溶液中のNH3が発生する弱塩基遊離反応が完了後、加えたNaOHは溶液中に残存する。
NH4+は、水溶液中でH2OにH+を
与える反応を起こし、
ブレンステッド説では酸として働きうる。
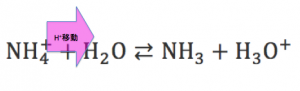
①の反応が②の反応より先に起こるのは、
酸の力がHCl>NH4+で
“強い”ものが優先反応したからである。
と言う事で、HCl+NH4ClaqをNaOHで
滴定すると、
①HClによる強酸性
↓
②弱塩基遊離反応で生じたNH3の弱塩基性
↓
③NaOHによる強塩基性
という順序で溶液の液性は変化する。
これらを滴定曲線に表すと、下のようになる。
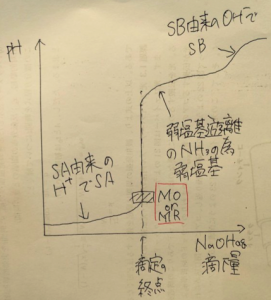
溶液中の強酸が反応完了する
(=NH3の逆滴定の反応の終点)
におけるpHジャンプで変色する
変色域を持つpH指示薬は、
右を見ると分かるように
メチルオレンジ(MO)もしくは
メチルレッド(MR)である。
いずれのpH指示薬を用いても、
滴定の終点は赤色から黄色に変化する事でわかる。
二酸化炭素の逆滴定
それでは次に二酸化炭素の逆滴定を話していきます。今回は二酸化炭素を溶かす溶液が水酸化バリウムで行うバージョンをやります。
水酸化ナトリウムバージョンってかなりややこしいんですよね。二段滴定をまずわかってくれないことには話になんないんですよ。
ちなみに、二酸化炭素の逆滴定は3種類あります。
「水酸化バリウム」で滴定するパターンが1つと、「水酸化ナトリウム」で滴定するパターンが2つあります。
水酸化バリウムで滴定する
二酸化炭素の滴定をしたいならば、これが一番簡単です。なぜなら、
Ba(OH)2+CO2→BaCO3+H2O
この反応の炭酸バリウムが沈殿するんです。てことはやで、
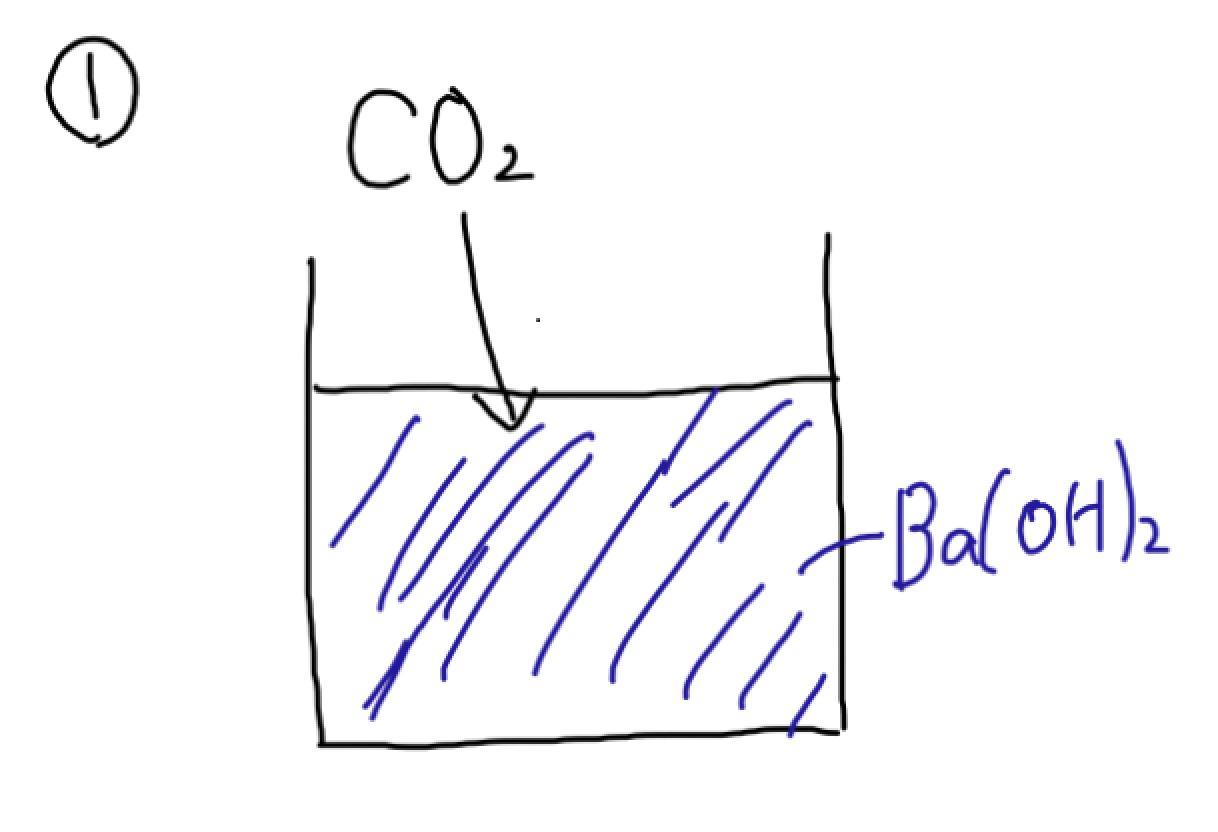
まず、こんな感じで二酸化炭素を過剰量の水酸化バリウムにくぐらせます。
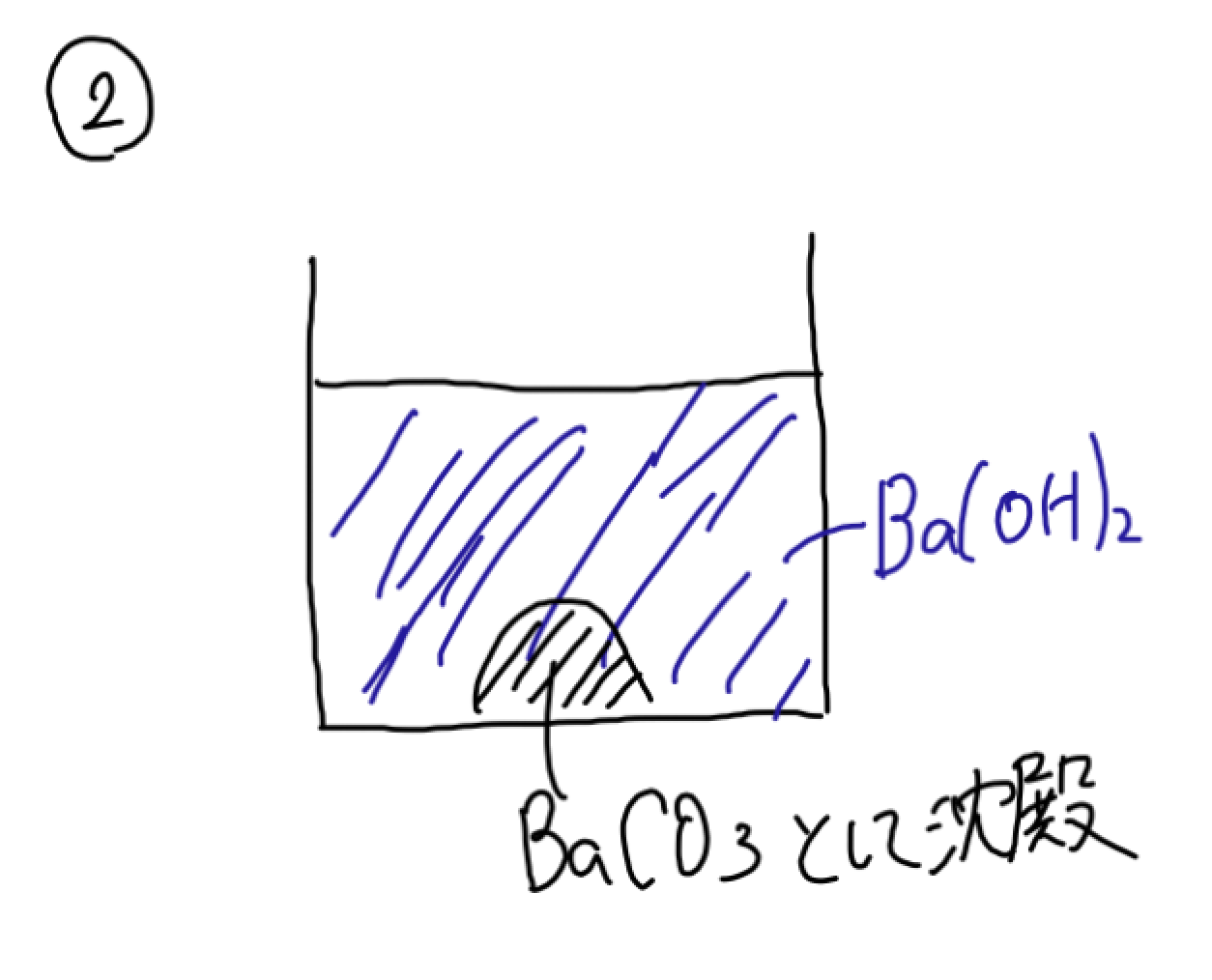
そうすると、炭酸バリウムが沈殿として落ちます。
それを取り除いてHClで余っている水酸化バリウムのモルがわかれば、引き算で二酸化炭素のモルがわかります。なので、イメージはしやすくなりますよね。
SO42-、CO32-の陰イオンに対してBa、Ca、Pbが組み合わさった時です。
計算での注意点
二酸化炭素の逆滴定はイメージするのは簡単なんですが、計算でミスりやすいです。その理由は登場人物が、二酸化炭素と水酸化バリウムと塩化水素ということで、二価と一価が混ざっているからです。
だから難しい!
でも大丈夫!逆滴定とかなんかかっこいい名前ついているから、気負ってしまう人もいるかもだけど、言っても中和反応ですからね。中和反応といえば、どういう式を作ればいいのか覚えていますか?
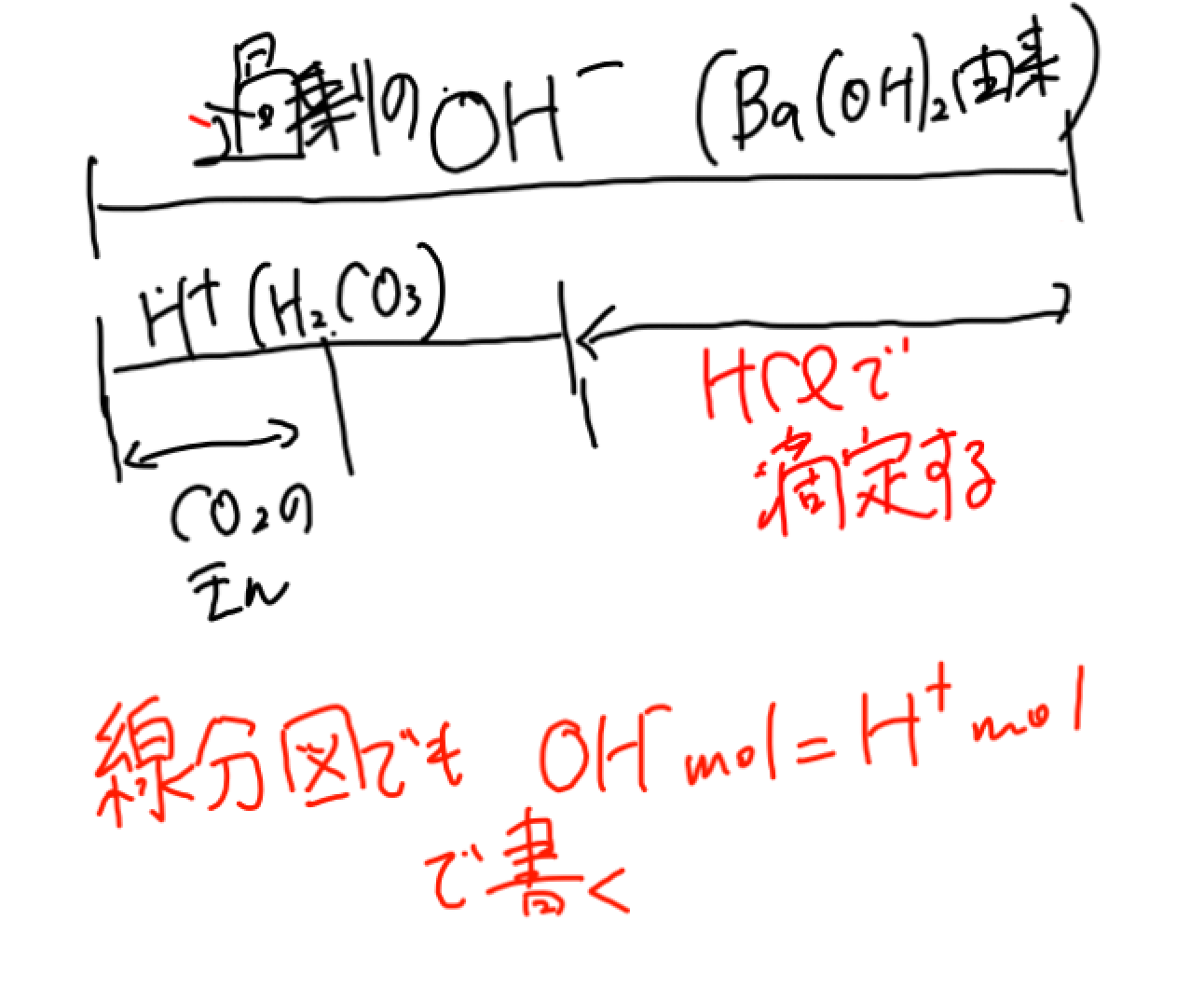
中和の量計算は全てH+mol=OH–molで行けたわけですよ。なので逆滴定の計算方法の「線分図」にそれを当てはめます。
二酸化炭素の逆滴定の例題
ある量の二酸化炭素を、0.10mol/Lの水酸化バリウム水溶液50mLに完全に吸収させた。この溶液を十分静置して、生じた固体を沈殿させた。この上澄み液10mLをとり、残った延期を0.10mol/Lの塩酸で滴定したところ12mLを要した。吸収させた二酸化炭素の物質量はいくらであったか。
出典:新研究化学I IIp262
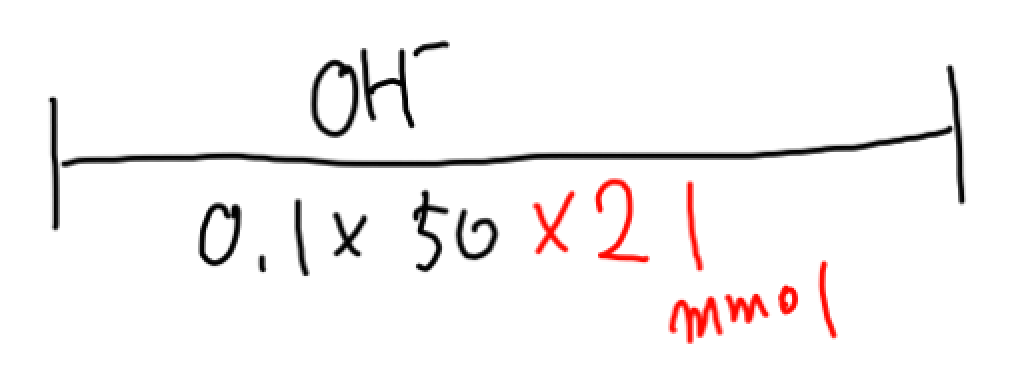
まずOH-は水酸化バリウム由来ですので、水酸化バリウムのモルの2倍あります。
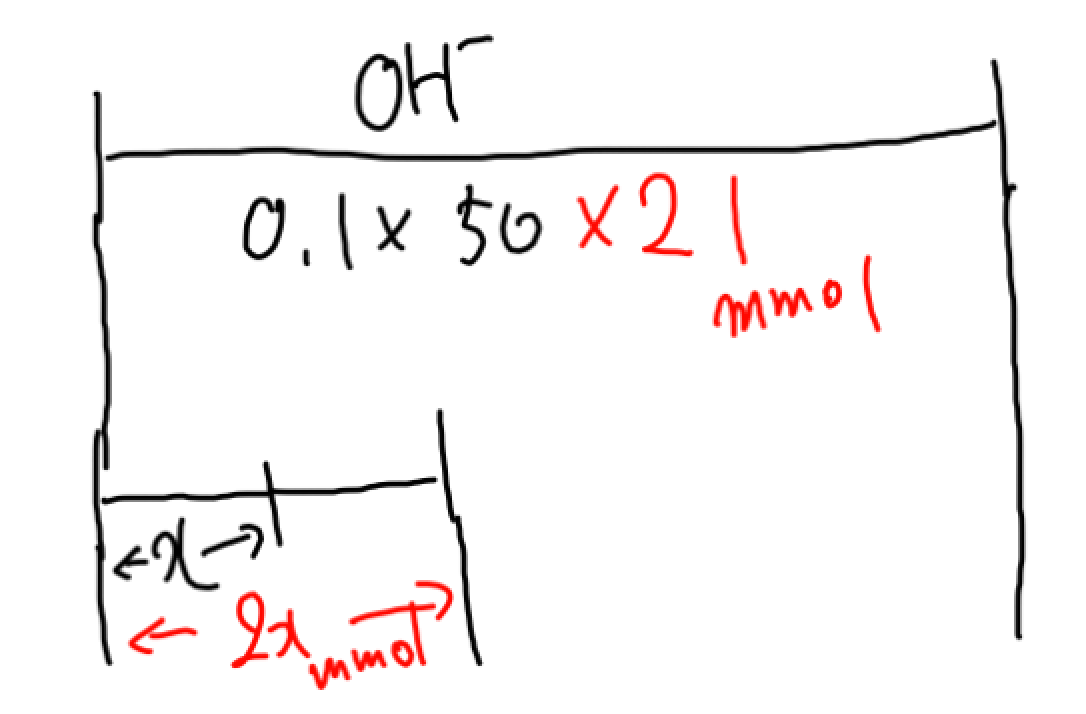
二酸化炭素そのOH-のうち求めたい二酸化炭素の物質量をxmmolとすると(あえてミリモルにしてます)、OH-を2xmmol消費します。
そして残った部分を、HClで滴定します。

この線分図をそのまま式にしちゃいますね!
0.1×50×2=2x+0.1×12×1×5
デートコンテンツを作るためにデートしなければならないのは当然ですよね。
よって、x=2.0mmol=2.0×10-3mol
となります。
二酸化炭素の逆滴定で水酸化ナトリウムに二酸化炭素を溶かすパターン
最初に表を見せたと思いますが、Ba(OH)2を使わずにNaOHを使うパターンが2つあります。この2つは、ワルダー法とウィンクラー法という名前が付いているんですが、ワルダー法はかなり難しいです。
ワルダー法ができれば中和滴定で怖い問題はまずないですね。
最後に
逆滴定って結構難しいと思っていた人も多いとは思いますが、結局酸塩基なんてものは、全てH+mol=OH-molの計算で型がつきます。
ややこしい問題こそ、基本に立ち返る大切さが分かったと思います。なんども復習してみてくださいね!では!













サイトの上の方で、「このように水酸化ナトリウムや水酸化バリウムなどのような強塩基を使えば、二酸化炭素と中和反応をしてNa2CO3やBa2CO3として溶液中にとどめておくことができます。」とありますが、Ba2CO3ではなくてBaCO3ではないですか?
ありがとうございます。
なぜ二酸化炭素は2xmmolなのですか。
二酸化炭素は二価の酸だから
セミナーの例題でつまってたところがこの解き方でやったらすんなり理解できました。ありがとうございます
よかったです!
上澄み液が60mlとわかっている理由がわからないです。
例題は、はじめ二酸化炭素を通してできた上澄液を10ml取るところを取らずに50mlを塩酸で滴定するとして考えやすくしている、と言う理解でよろしいですか?
上澄み液の物質量を5倍するのはなぜですか。
上澄の5分の1を取り出してるから元に戻しただけです。