ボイルの法則って難しいですか? ボイルの法則自体が理解できない人ってほとんどいないんですよ。
圧力が大きいってことは、体積が小さくなるってことですからね。PV=一定だと。
じゃあ、これがわかった人がいざ重要問題集を開いて計算問題に取り組んだら解けるのか? っていうと全く解けないんですよ。特に気体の問題で重要問題集B問題になるとほとんどの人はお手上げなはず。
結論から言うと、ボイルの法則を意識して入試問題を解くことはありません。
「気体の圧力を2倍にしたら体積が1/2倍になるから、圧力と体積の積が一定なんだ!」
こ~んな風に覚えようとしていませんか?
こんなこと覚えてても糞の役にも立ちません。むしろボイルの法則などを覚えようとすると、うまくいかない。
今回の記事では、一応ボイルの法則について解説します。しかし、メインはボイルの法則は「いらねえ」ってことの説明に時間を掛けます。
ボイルだけ知りたい人は、途中で離脱すればいいでしょう。演習問題をバッチリ解いて入試で問われる気体計算問題をバッチリ解けるようになりたいなら、ボイルの法則はなぜ要らないのかまで読んでいってください。
多分、気体分野に悩んでいる人にとってはちょっと革命が起きるかもしれません。
目次
ボイルの法則とは?当たり前すぎるこの法則を具体例でわかりやすく説明してみた

この図のように、
ボイルの法則はPV=k(一定)で表されます。この式が表すのはまさに上の図に書いてある通り。てことは、式変形で

または、

と表すことができます。
反比例なので、圧力が大きくなれば、体積が小さくなり、体積が大きくなれば圧力が小さくなるってことなんです。

って思いませんでした? 高校生の頃の僕はそこが疑問に思って、どんどん気体がわからなくなっていきました。

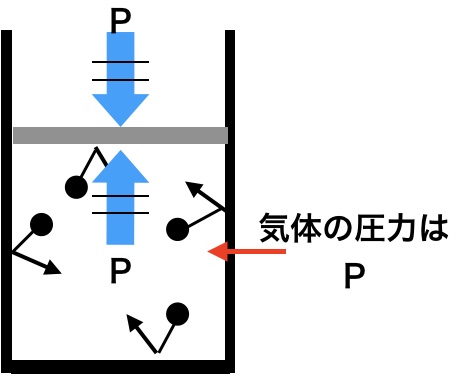
てことは、つまり外側から押されている圧力がPならば、ピストンの内側の気体が押し返す力もPである。
【衝撃】ボイルの法則を覚えるのは気体に苦手意識を持つ諸悪の根源
気体の問題得意な人あるある
・ボイルの法則
・シャルルの法則
・ボイルシャルルの法則入試問題でつかったことない。
— 受験化学コーチなかむら (@kagakucenter) 2018年10月14日
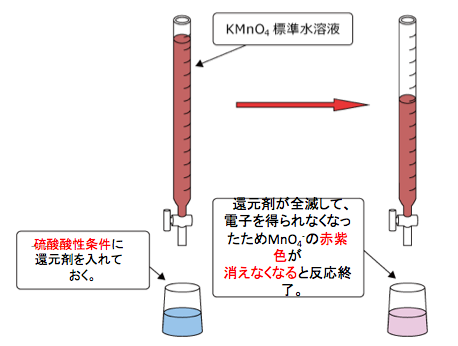
すみません。ボイルの法則解説したんですが、基本入試では使わないので忘れてください。
厳密には、使うんですがボイルの法則を使おうと考えたことはありません。結果的にPV=一定という関係式を使うだけです。

といちいち考えることはありません。
受験化学を三年以上教えていると流石に傾向がわかって来ます。
気体分野、混合気体は100人中98人は苦手に思うんですよ。その理由が、ボイルの法則とかシャルルの法則に縛られているからなんです。
多くの受験生は、

って悩むんですよ。僕から気体を学んでいる人は、一切こんなことを考えませんよ。
その理由はこちら。
ボイルの法則は結果論である。気体の問題の解き方

結論から言うと、使うのは状態方程式のみです。いちいちボイルの法則だとか、シャルルの法則だとか分類しません。
実際の具体例を出してどのように計算するのかを解説していきましょう。
温度Tで、1.0×105Paで2Lの気体は、温度T,5.0×105Paでは何Lを占めるか。
ステップ1:図を描く

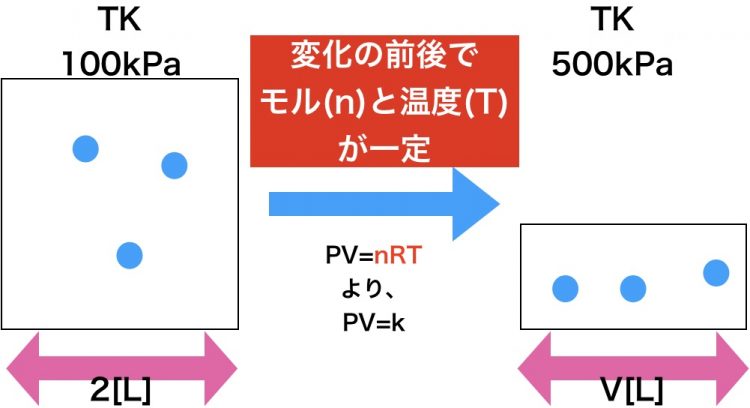
このように、変化の前後をそのまんま図にします。ちなみに、四角の中の青い丸は、気体粒子を表しています。数は適当ですが、変化の前後で数が変わっていないことが重要です。
図が2枚あるときは、変化の前後で何が一定で変わっていないかを確認します。
この図だったら前後でモルと温度が一定です。
ステップ2:n,T一定なので状態方程式の気体定数Rとまとめる
PV=nRTのうちn,R,Tが変化の前後で一定なんですよ。てことは、定数としてkでまとめます。
すると、現れてくるのが
PV=k
という関係式なんですよ。
ここまでわかりますか?
つまり、僕はボイルの法則を使おうとして使っているのではなく、図を書いて結果的にボイルの法則を使っているのです。
PV=一定は使えるかな〜と問題文を読むのではなく、問題文を図に表しているうちにPV=一定が浮かび上がってくるっていうイメージです。
もちろんね、こんな問題ボイルの法則に決まってますよ。図を描くのはだるいですよね。
でもね、入試問題でこんな簡単な問題出ませんよ。入試問題は99%混合気体ですよ。
気体の種類が2種類以上。さらに、その気体が燃焼反応したり、水に溶けたり、蒸発したりいろんなことを考えないといけないんですよ。
そんな時に、図を描かないとはっきり言って入試の気体問題に歯が立たないんですよ。
なので、このように図を書いてどの関係式を使えばいいのかっていう解法は必ず身につけてください。この解法は僕のメルマガで動画講義しています。
正直、最低限図の解法を身につけないと混合気体は絶対に解けないです。
発展:入試でボイルの法則を一番使うのは分圧⇔分体積変換

入試問題で一番ボイルの法則を使うのは、分圧と分体積の変換です。
おそらく、「ボイルの法則」と調べている人は、混合気体までしっかり理解していないと思われます。
ですが、いずれ必ず学ばなければならないことなので、今まだわからない人は、この記事をブックマークしておいて、いずれ必ず読んでおいてください。
まとめ
- ボイルの法則は、押せば体積が減ると言う至極当然のことを数式にしたもの
- ボイルの法則を覚えていても計算には一ミリも役に立たない。
- 気体は図をかく。
とにかく、気体の分野は苦手な人が死ぬほど多い分野です。
そして、苦手の第一歩がボイルの法則、シャルルの法則を覚えることなんです。気体の法則を覚えても何一つ悪いことはありません。