こんにちは。




水酸化鉄(III)コロイド溶液には下のような特徴があります。
- 理科室での調整が容易
- 鮮やかな赤色だから観察しやすい
- 疎水コロイドなので、少量の電解質を加えるだけで沈澱を生じる(凝析)
これが実験でよく使われ、テストにもよく出る理由です。
この記事では水酸化鉄(III)コロイド溶液の化学的な性質や、様々な実験における反応を徹底解説します。
しっかり対策しておけば、得点源になること間違いなし!
目次
水酸化鉄(III)コロイド溶液の分類と性質
水酸化鉄(III)(Fe(OH)3)は水に不溶です。
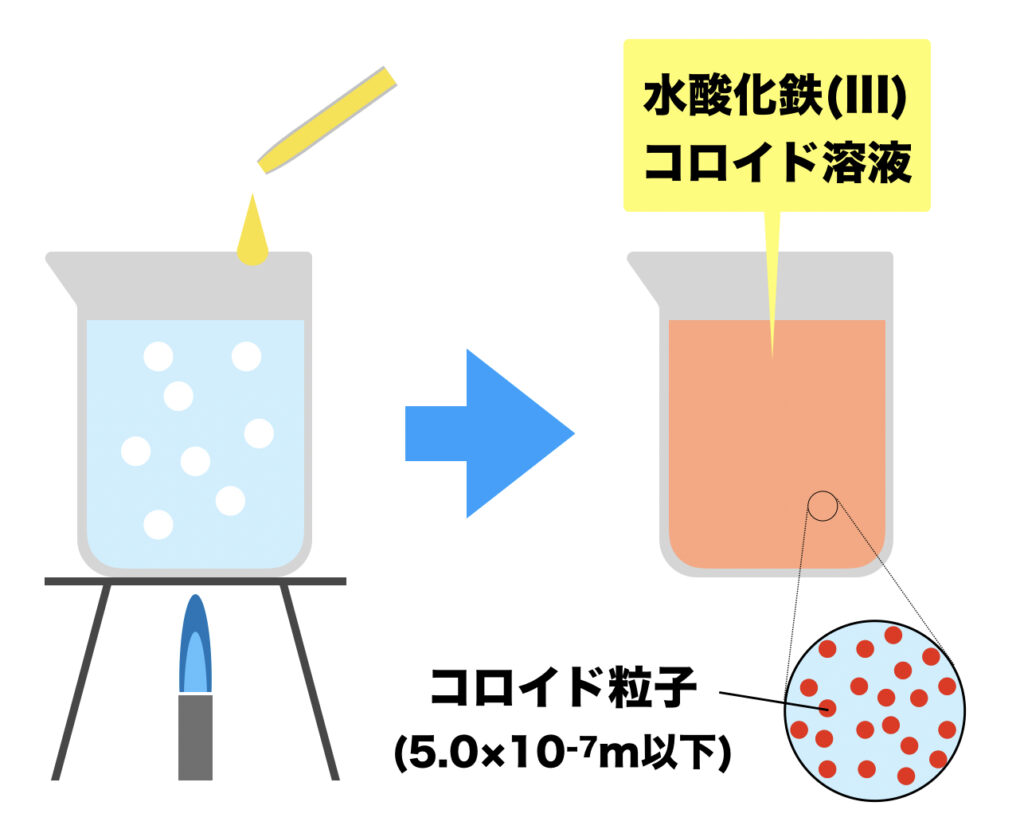
しかし粒子のサイズが5.0×10-7m以下の場合、水酸化鉄(III)はコロイド粒子となり水中に均一に分散します。
このように水に不溶のコロイド粒子が溶液中に分散したものは分散コロイドとよばれます。
また分散コロイドは水との親和性が低いので疎水コロイドとも言われ、少量の電解質を入れただけで凝析し沈澱を生じます。
水酸化鉄(III)コロイドは電離してイオンにはなりません。
しかしOHの部分がわずかに負の電荷を持ち陽イオン(Fe3+やH+など)を引きつけるので、全体として正の電荷を帯びます。
このようなコロイドを正コロイドといいます。このようにコロイドが正、負の電荷を持つ理由を「「コロイドが電荷を持つ理由」と「正コロイド・負コロイドの見分け方」を徹底解説!」で解説しました。詳しくはこちらをご覧ください。
正コロイドは、価数の大きい陰イオンを持つ電解質によってより強く凝析します。
つまり電離してClーを生じる塩化バリウム(BaCl2)より、SO42ーを生じる硫酸ナトリウム(Na2SO4)を加えた方がより凝析するのです。
- 分散コロイド…水に不溶の粒子が分散
- 疎水コロイド…少量の電解質で凝析
- 正コロイド…正の電荷を帯びている
コロイドの種類と性質についてより詳しく知りたい人は、こちらの記事も読んでみて下さい。
水酸化鉄(III)コロイド溶液の調製方法
では、どのように水に不溶の水酸化鉄(III)をコロイド粒子サイズにするのでしょうか?
これは「化学反応が急速に起こる」ためです。
沸騰させた純水(H2O)の中に、水に可溶である塩化鉄(III)(FeCl3)の飽和水溶液を少量加えます。
すると下のように反応し、水に不溶の水酸化鉄(III)(Fe(OH)3)を生じます。
FeCl3 + 3H2O → Fe(OH)3 + 3HCl
この反応は非常に短時間で起こるため、水酸化鉄(III)の結晶は大きく成長できずコロイド粒子サイズになります。
この結果、赤色の水酸化鉄(III)コロイド溶液が出来るわけです。
沸騰している純水の中に、塩化鉄(III)の飽和水溶液を少量加える。
FeCl3 + 3H2O → Fe(OH)3 + 3HCl
水酸化鉄(III)コロイド溶液の透析実験
調製した水酸化鉄(III)コロイド溶液を半透膜であるセロハンの袋に入れ、純水中にしばらく浸します。
その後セロハン袋のまわりの水を少量試験管に取り、リトマス紙で液性を調べると「酸性」になっています!
また硝酸銀水溶液(AgNO3aq)を数滴加えると、塩化銀(AgCl)の「白色沈殿」を生じます!
これはセロハン表面の小さな穴を通って、水素イオン(H+)や塩化物イオン(Clー)がセロハン袋の外に出てきたために起こった現象です。
水素イオンによって水が酸性になり、塩化物イオンと銀イオンが反応し沈澱が生じたんですね。
しかし、水酸化鉄(III)コロイドはセロハンの穴より大きいので外に出てきません。
なので外の水は透明なままです。
このようにセロハンなどの半透膜を用いてコロイド溶液に含まれるイオンや分子を取り除く操作を「透析」といいます。
調製したコロイド溶液をセロハン袋に入れ純水中に浸す
⬇︎
水素イオンと塩化物イオンが袋の外に出てくるが、水酸化鉄(III)コロイドはセロハン袋内に残る=透析
⬇︎
セロハン袋の外の水は酸性になり、硝酸銀水溶液を加えると塩化銀の白色沈殿を生じる
名前の似ている透析・凝析・塩析の違いについてはこちらの記事も読んでみて下さい。
水酸化鉄(III)コロイド溶液の電気泳動実験
水酸化鉄(III)コロイドは正の電荷を持つ「正コロイド」です。
したがって電圧をかけると、コロイド粒子は陰極側に引っ張られて移動します。
この現象を「電気泳動」といいます。
水酸化鉄(III)コロイドは正コロイド
⬇︎
電圧をかけると陰極側に移動する=電気泳動
水酸化鉄(III)コロイド溶液のチンダル現象実験
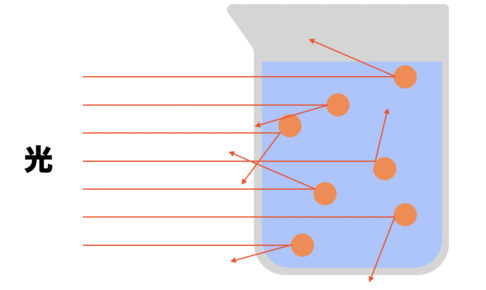
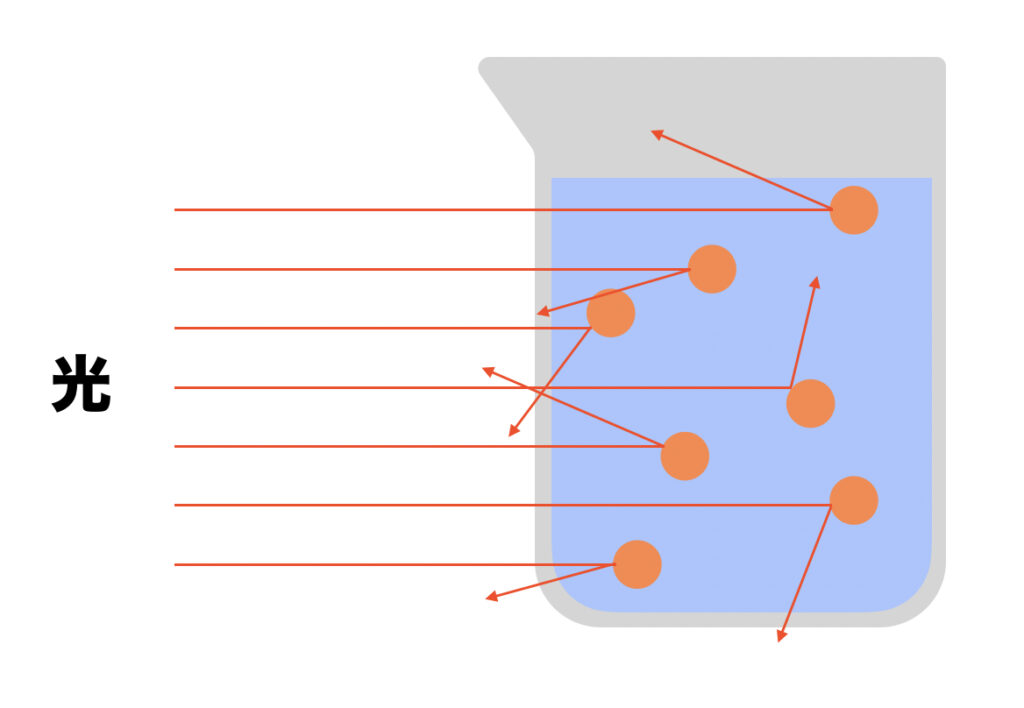
コロイドの共通性質であるチンダル現象を用いて、水酸化鉄(III)コロイド溶液がコロイドであることを確かめる実験がよく行われます。
横から強い光を当てるとコロイド粒子は光を散乱させるので光の通り道がはっきり見えるのですが、真の溶液では見えません。
コロイド粒子が光を散乱するので、光の通り道が見える。
まとめ
<分類>
- 分散コロイド
- 疎水コロイド
- 正コロイド
<調製>
- 沸騰した純水に塩化鉄(III)水溶液を加える
<実験と結果>
- 凝析実験…少量の電解質で沈殿を生じる
- 透析実験…セロハンを通れない イオンは通る
- 電気泳動実験…陰極側に移動する
- チンダル現象実験…光の道筋が見える