こんにちは。


このような状態になっていませんか?
実は気体の問題をスッキリ理解して、初めてみた問題でもスッキリ解くことができる方法があります。
それが状態方程式から関係式を導き出す方法です。
多くの人が気体が難しく感じ、問題集で暗記した問題しか解けないのは、ボイルの法則、シャルルの法則、ボイルシャルルの法則、アボガドロの法則、など個別にいろんな気体の法則を覚えているからです。
今回の方法で少なくとも気体の問題を「覚えて解こう」と思うことは無くなるでしょう。むしろ覚えないことで、状況把握が徹底的にうまくなります。

状態方程式毎回といてたら、いくら試験時間があっても足りませんわ(笑)
だから、どのようにして気体分野の入試問題を解いて行くか、気体の法則をどう使うか、超実践的な使い方をあなたに使いこなせるようにしていきたいと思います。
目次
覚えるべき状態方程式
状態方程式は、おそらく知らない人はいないと思います。PV=nRTですよね。これは普通に覚えている人は多いと思います。
でも、問題を解く上では、もう一つの状態方程式を覚えておくとめちゃくちゃ便利なんです。なので、これもついでに覚えておきましょう!
もう1つの状態方程式も導き出すとかではなく、暗記しておいてください。
意外とよく使いますし、かなり便利です。
覚えている事によって、
「あ、これは状態方程式で求められる!」
と思いつく事もあります。
その状態方程式がPM=dRTです。(M:分子量,d:密度)
モル数n=w(質量)/M(分子量)なのは大丈夫ですね!そして、これを代入して
PV=wRT/M
両辺Mを掛けて、Vで割ります。
すると
PM=(w/V)RTとなります。
(w/V)は単位体積辺りの質量だから、
これは密度dです。
よってPM=dRTとなります。この状態方程式も必ず覚えておいてください。
状態方程式と各気体法則の関係

ボイル、シャルル、アボガドロの法則と気体の状態方程式PV=nRTの関係は上のベン図の用になります。
つまり!
ボイル、シャルル、アボガドロの法則は、気体の状態方程式PV=nRTが確立された現在からみれば、
状態方程式の中で定数をまとめてkとおくことにする。
ボイルの法則はPV=nRTでn,T一定の時、定数はnRT。だからPV=k。
シャルルの法則はPV=nRTでP,n一定の時、定数はnR/P。だからV=kT(体積は絶対温度に比例する)。
アボガドロの法則はPV=nRTでP,T一定で、定数は、RT/P。だからV=kn(体積はモルに比例する。)。
| 法則名 | 条件 | 公式 |
| ボイルの法則 | n,T一定 | PV=k |
| シャルルの法則 | P,n一定 | V=kT |
| アボガドロの法則 | P,T一定 | V=kn |
これって、状態方程式覚えておけば全部いけるんじゃないですか?やった〜!気体の法則なんて覚えなくていいんだ!!
いや、実はそうじゃない、アホみたいな参考書は「全部状態方程式で求めろ!」と書いてあるけど、これは絶対にやめてね。実は問題点があるんだ。
ちなみに、ボイルの法則とかシャルルの法則は覚える必要はないからね!
まあ、PV=kがボイルの法則とか、V/T=kがシャルルの法則だ!ってことは覚えるとは思うけど、
「n,T一定の時は、ボイル」「P,n一定の時は、シャルル」って覚えるんじゃなくて、毎回導出するってイメージが正しいですね!
だって、時々「V,n一定で、P/T=k」という関係式を使うことだってありますからね!これ何の法則?って聞かれても答えが出ないですよね。
法則の暗記はむしろ害悪です!
状態方程式の問題点
状態方程式には大きな欠陥があります。この欠陥を無視して、状態方程式だけで解くことはできません。
理論化学の基本は『モルを使え!』でした。だから、

と求めようと思うのが自然ですね!ですが、状態方程式の欠陥は、状態方程式はPV=nRTの気体定数R以外は変数であるということです。
つまり、状態方程式は『分からない事だらけ』

式中に4つも変数があり、このまま計算する時間がかかって仕方が無いんです!こんなもの、全部使っていたら、まあどんなに優秀な人でもいつか、計算ミスをします。
だから、気体分野の問題を解く上で最大の方針は、
です!
確かに、状態方程式は万能ですが、こういう気体の問題では、“積極的に気体の法則を使う必要がある “のです。
気体の法則は、変数を減らす作戦なんです。そして、状態方程式というのは、割と苦肉の策ってことを覚えておいてください。
でも、気体の法則って必ず使えるものじゃないんですよね〜。
例えば、n,T一定って当たり前のように書きました。でも、
何と何の間で一定なやねん!!??
って思いません?
実はこのツッコミ欲しいんですよ。一定ってどういうこと?
この”一定の意味”がわかれば、気体の問題を解くのに、非常に有効です。
この気体の法則の「一定」っていうのは、一定っていうのは、変化前後なんですよ!!
つまり、ですよ!!!問題文で変化があった時何かしら「一定」のものがあるんですよ(入試問題では必ずあります)。なので、その一定のものを決して、気体の法則を使うんです!!
はい、このチャプターで1、2を争うくらい重要な事言いましたよ〜!ノートが燃えるくらいメモ取っておいてくださいね!笑
気体の問題の解き方~状態方程式の変数の減らし方~
気体の問題は、みんな苦手です。なぜなら、問題文に腐る程データが出てきます。なので頭がこんがらがります。
なので、気体の問題では、問題文を必ず図にするという習慣をつけてください。頭の中でできると思わないでください。
この図を考えることで、問題の解き方も図が教えてくれたりするんです。
今回話す、「図にする」という技術は、絶対に気体、混合気体の間に身につけてくださいね。脅すわけじゃないですけど、
気体、混合気体ができないと、ヘンリーの法則は死ぬし、蒸気圧も死ぬし、気体平衡も死ぬんです。
ヘンリーの法則がわかりません!っていう質問のほとんどが混合気体がわかっていないことがほとんどです。
蒸気圧の質問が来たとしても、ほとんどが混合気体がわかっていないことによる質問です。
なので、その混合気体を解くためにも必ず図を書く癖をつけてください!
さらにこの図のある事に着目すればこの問題ではどういう事をすればいいか一瞬で浮かび上がります。
そのあることとは、
「図の個数に着目する」
です。
さっきも言いましたが、変化がある時は
問題文を図に表して、、その個数が、、、
1個なら⇒状態方程式に代入!
2個以上なら⇒一定をkにまとめて気体の法則で解く!
じゃあ、どういう図を書けばいいのかを考えていきましょう!例題を出します!
例)ある気体Xは、27°C=300K、1.0×105Paにおいて物質量が1mol気体定数8.3×103(Pa・L)/(mol・K)、密度2.4g/Lとする。気体の分子量を求めよ。
この問題では次のように図を書いてください。
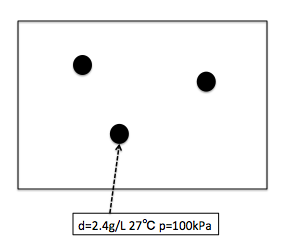
ポイントは粒まできっちり書くというところにあります。この粒の数がモルの変化をしているかしていないかを表現するのに必要だからです。
そして、先ほどの述べた問題を解く方針から考えると、図は状態が変化していないので、1枚しか書けません。
つまり状態方程式を使うという事です。
本問は気体の密度が欲しいので、密度が式の中にあるPM=dRT式に代入します。

それでは次は図を2枚のバージョンをやっていこうと思います。
容積一定の容器にN2を封入して、100kPa、27℃であったのを87℃の間で加熱した。加熱後の圧力を何Paか?
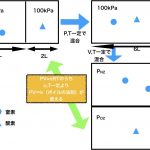
本問の内容を図示すると、下のように図が2枚書けます!「容積一定」というヒントから、同じ体積の図を書いてくださいね!あと、モルが絡む時は、粒も書いておくといいでしょう。
今後は、こういう気体が燃焼反応をしたり、別の種類の気体が混ざったり(混合気体)しますので、気体粒子を書く癖はつけたほうがいいですね。

こういうときにn,Vが一定なことは、そして、kにまとめて状態方程式の変数を消して行きます。
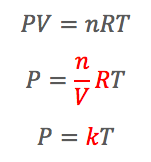
一定のものをRとまとめてkにしてしまいます!
これよりp/T=kという関係式が成り立ちます。
さあ、ここで、おもいだしてほしいのですが、この式ってボイルですか?シャルルですか?アボガドロですか?
実はこれに当てはまる法則名が無いんです。ね!さっき言ったやつですよ。
だから、気体の法則の名前とか公式自体は覚える必要はないと言ったのです。実際に図を書いて状態方程式から使う式を毎回作り出すのです。
この図を書いて変化の中で一定な物をまとめて、関係式を作り出せれば、気体の法則は覚えなくてもいいのです。
では実際に後は代入するだけです。
これより、

これを解いてP=120kPaとなります。
まとめ
状態方程式は変数が劇多なので、なるべく使いたくありません。なので、状態変化だったり、化学変化だったり、変化がある場合は、変化前後で一定のものを探しましょう!
一定のものをまとめてkにして、気体の法則を毎回作ればいいんです!!
気体の法則は覚えると応用が効かなくなるので、覚える必要はありません。
「あ、結果的にボイルの法則だったな」
という感じでいいのです。
そして、図を書くということはめっちゃ大事なんで、100%図を書くことを忘れないでくださいね!混合気体になった時、頭の整理にめちゃくちゃ役に立ちます。
では、次に混合気体の問題に挑戦していきましょう!!!















お世話になっています。しかし、こちらの気体の法則に関してはまったく知らずに(見落として)いました。目から鱗。助かりました。ありがとうございます。
どうして、RもnとVと一緒にまとめることができるのですか? また、Rをまとめない場合はどのようなときですか?
全部定数だからです。Rをまとめないことはありません。気体定数だからです