こんにちは。
なんか試験時間内に全然終わらないんですけど、、、
化学って有機をやっていると、
集中しちゃって、
周りが見えずに、いつの間にか
試験中スゴい時間が経過、、
ということはよくあるよね。
しかも、計算も難しくなると、
ごちゃごちゃになって、
計算ミスが
ないように見直ししながら
進むと、
とてもじゃないけど全部
終わらないんですよね〜
本当にこれはよくわかります。
せっかく内容を理解して来たのに、実際試験になると時間に縛られ、内容がわかったとしても、解ききれずに終わるという悔しいこともよくあります。
なので、今日は、すこしでも、この「試験時間が足りない」という悩みを解決できるよう、とある計算を早くするツールをお渡ししたいと思います。
目次
最強の楽々計算ツール

この章では、多くの受験生が使えていないマル秘ツールをご紹介します。
普段からよく目にするものですが、なぜか受験化学ではほとんど使われていません。
このツールを使うとより速く、より正確に計算する事ができます。
そのツールとは、、「補助単位」です!
言葉で言われても分からない人もいるかもしれません。
補助単位とは、kgやhPaなどのkやhの事です。10の何乗かをあらわしていて、日常生活でもよく使いますよね。

とは言わないですよね!30kgって言います。この「k」を使いこなすのです。
補助単位はとても重要で、
h:ヘクト:やk:キロ:などがあります。
これを計算の中で使っていくと計算で非常に重宝します。
例えば、中和の問題では、
「0.05mol/Lの硫酸55.0mL」など、
mol濃度の単位がmol/Lにも関わらず、体積がmLで与えられるときです。
ていうか、中和滴定の問題などではまず、Lではなく、mLで与えられます。
その場合下のように計算してしまいます。
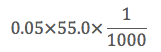
こうやり、molに変換して
計算します。
これが間違いというわけでは
ありません。
ですが、
これが滴定問題だったらすごい手間ですよね。
硫酸を中和するNaOHのもmolに直す、
そして弱塩基のなどもmolに直すなど、
計算過程が多い事で、
どこかでミスをしてしまう可能性が、
非常に高くなります。
実は、でもあなたは悪くありません、
なぜなら、あなたが勉強している
問題集や教科書、授業をする先生が
悪いのです。
下の画像をご覧ください。
これは多くの高校で使われている、
セミナーの解答です。

そりゃ、みんな
このやり方やっちゃうでしょ、
これを解消するのが
補助単位m(ミリ)です。
このようにミリをのこし
てmmolで計算していくのです。
この補助単位は分野に関係なく、
出て来たら必ず使えます。
そして、化学計算の桁数間違いが
格段に減ります。
そして、
より正確に、
より速い計算が可能になります。
もう1つの使用例
とりあえず、この記事では、
もう1つの補助単位の使い道を
載せておきます。
これはかなり強力な力に
なります。
それが気体分野です!
気体分野ではよく、
という与えられ方がメチャクチャ多いです。
ですが、
このまま計算すると、
![]() がずっとつきまとってだるいです。
がずっとつきまとってだるいです。
だから、こういうときは、
のように、kPaを使います。
これを使えば、累乗を残さず
計算できますし、
他にもう1つかなり便利な
事が起きるのです。
それが気体定数の累乗も無くなる
ことです。
気体定数の数値と単位を
キッチリ見て行きましょう。

このようになっております。
ここで、キロパスカルを使うと、

いったん10^3を分子に上げて、
10^3Pa=kPaと変換します。
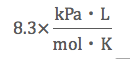
『メチャクチャスッキリ!』
気体の問題は、kPaを使えば、
一気に気体定数まですっきりするので、
非常に有効な方法なのです。
俺のメルマガ講座でも補助単位を
用いて気体の問題を解く方法も
公開しているので、
是非この記事の下の方の
無料プレゼントを受け取ってください。
補助単位一覧表公開!
これを一覧にしておくので
一気に覚える必要はありませんが、
かならず計算問題で使った方がいいです。
ミスが減って、
正確に計算が出来る、使わない理由が見当たらない!
| 補助単位 | 読み方 | 値 |
| k | キロ | 103 |
| M | メガ | 106 |
| G | ギガ | 109 |
| T | テラ | 1012 |
| 補助単位 | 読み方 | 値 |
| m | ミリ | 10-3 |
| μ | マイクロ | 10-6 |
| n | ナノ | 10-9 |
| p | ピコ | 10-12 |
それでは是非あなたの
化学計算に取り入れてください。
それではありがとうございました。

















はじめまして
この度合法カンニングペーパーをダウンロードさせていただきました。とてもわかりやすい解説でこれからの化学の勉強が大いに捗ると思いました。
ここで一つ疑問なんですが、濃度変換の合法カンニングペーパーの作り方がのっていて、色々試したのですが考え方が分からない問題がありました。
“2.00mol/Lの希硫酸51.4mLを作るのに必要な密度1.20g/mL,質量パーセント21.0%の希硫酸の体積は何mlか”
上記の問題において合法カンニングペーパーの方法で解くことは可能でしょうか?また可能なら解法を教えてくださいおねがいします。 長々とかいてすいません。
ありがとうございます!
ちなみにその問題は、ソモソモ硫酸のモルを=でつなぐだけの問題です。
これは”同じ溶液”の単位を変えているわけではなく、
この問題は、希釈して2mol/Lの硫酸を作っているわけですよね!だからこれは、単位を変換する問題ではありません。
分かりました!ありがとうございます。
このページを見て補助単位使い始めてから問題を解く速度が格段に上がりました!とても便利で愛用してます
よかったです!
今後もどんどん使っていってくださいね!