こんにちは。
今日は二段滴定について話していきたいと思います。
二段滴定って難しく考える必要は全くないですよ。中和滴定の一種です。ただ、ほとんどの人が難しくて難しくて震えているのは、炭酸ナトリウムの二段滴定なんだと思います。
ただ、実は、そんなに恐るに足らないんです。そのことをわかってもらうために、あえていきなり炭酸ナトリウムの二段滴定の話をしません。
最初は炭酸の二段滴定を理解してそのあとに、炭酸ナトリウムを勉強していきましょう。そうすると完全に理解することができるし、どんな問題でも解けるようになるでしょう。
ちなみに、この記事はこの動画で語れないくらい信じられない分量になります。最終的には炭酸ナトリウムの二段滴定を説明をしたいがために信じられない分量になりました。
目次
二段滴定とは?

二段滴定って何が二段なんか?
それは、滴定曲線が二段なのです。上の図は炭酸の滴定曲線を表しています。まず、例で酸を出しますが、ニ価の酸炭酸を考えてみます。
二価の酸である炭酸分子は、2箇所からH+が投げられますよね。
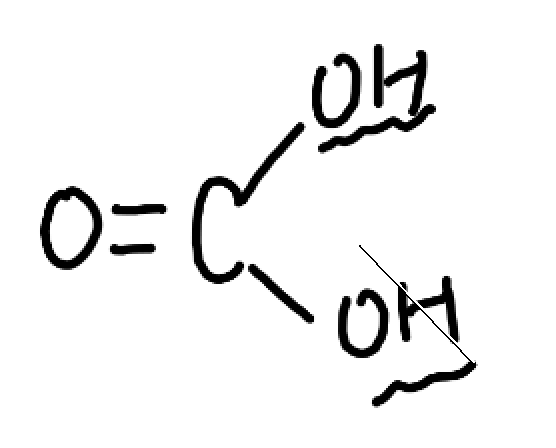
この2箇所って「電離定数」が違うんですよ。電離定数っていうのは、電離する力の序列。
ん〜わかりにくいって思った人は、H+を投げる順番だと思ったらいいです。この順番が決まっていて、2価の酸や塩基の電離定数って必ず1つ目と2つ目で差が出てくるんですよ。
伝説の強酸の硫酸でさえ第1電離と第2電離では、電離定数が違います。

電離定数に差があるから。
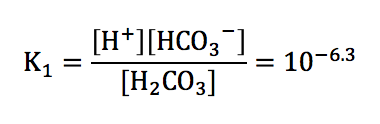

2価の酸や塩基は滴定曲線が
硫酸は二段滴定しないの?
硫酸も二価やないかい!硫酸は二段滴定しないんか?って思いますよね。二価やし。でも硫酸は二段滴定しません。希硫酸をNaOHで滴定した滴定曲線がこちら!

そう、こんな感じになるんですよ。なぜなら、硫酸の第2電離も普通に強酸だからです。つまり2価の酸やったら誰でも二段滴定できるってわけじゃないんです。
第1電離だけ終わった後の状態ってNaHSO4硫酸水素ナトリウムですよね。これ普通に強酸なんですよ。だからpHも小さい。よって滴定曲線も二段滴定になることはない。
ちなみに、硫酸の場合は、高校化学では電離定数を考えることはない。なんでかっていうと、硫酸は完全電離して不可逆反応をすると考えるから。でも厳密に言うと強酸でも電離定数は存在するし、強酸の中でも酸の強さの強弱がつくのは電離定数のせい。
結局二段滴定になる条件ってなんなの?
ここまで聞いて、バチっとわかった人も、う〜んて感じの人もいるでしょう。なので、どういう時に二段滴定になって、どういう時に二段滴定にならないのかをまとめようと思います。
そして、これがまとめ終わったらようやく炭酸ナトリウムの二段滴定に駒を進められます。
二段滴定になる条件は、
・電離定数の差が104以上あること
まず、2価じゃないと無理なのは説明不要ですよね。2箇所でpHジャンプを起こさないとダメなんだから、二価であることは必須です。
まず電離定数の差というのは、律儀に順番を守るかどうか?だと思ってください。
第1電離はお兄ちゃんで第2電離が弟だと思ってください。電離定数の差はH+を投げる順番をちゃんと守るかどうかだと思ってください。
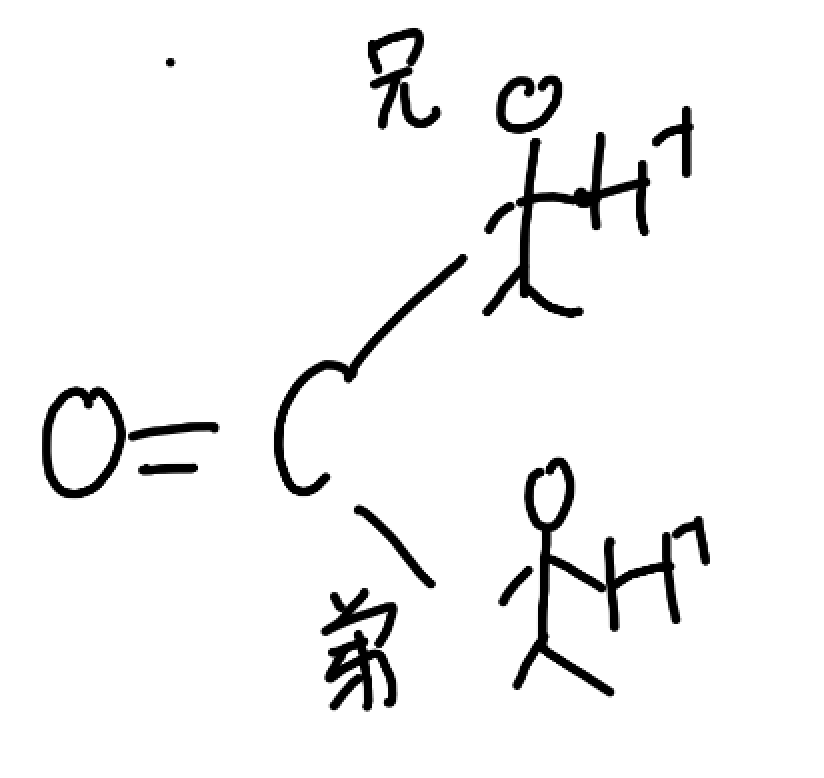
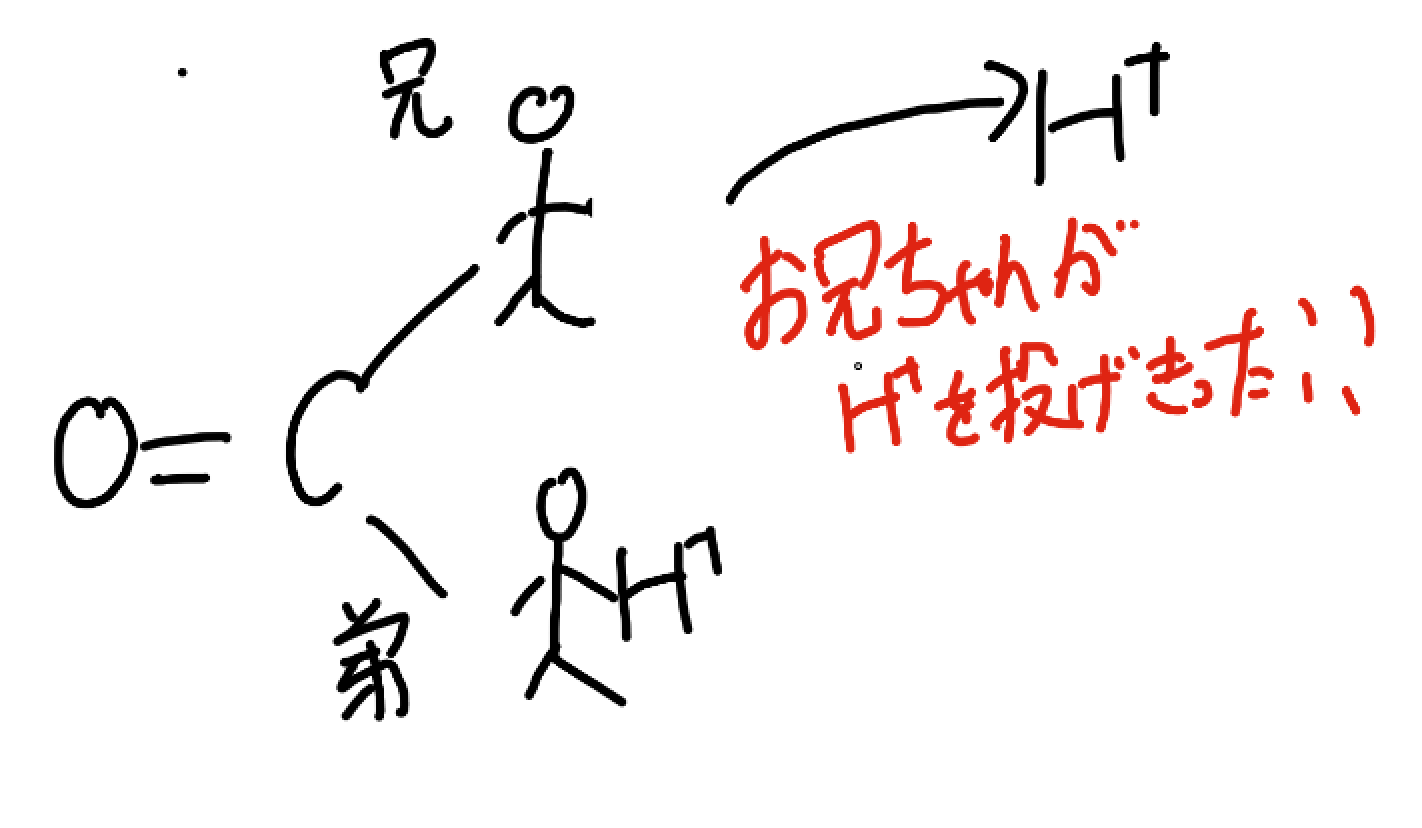

そう、このような投げ始めがくっきり別れるのが「電離定数の差が104」っていう数字なんですよ。
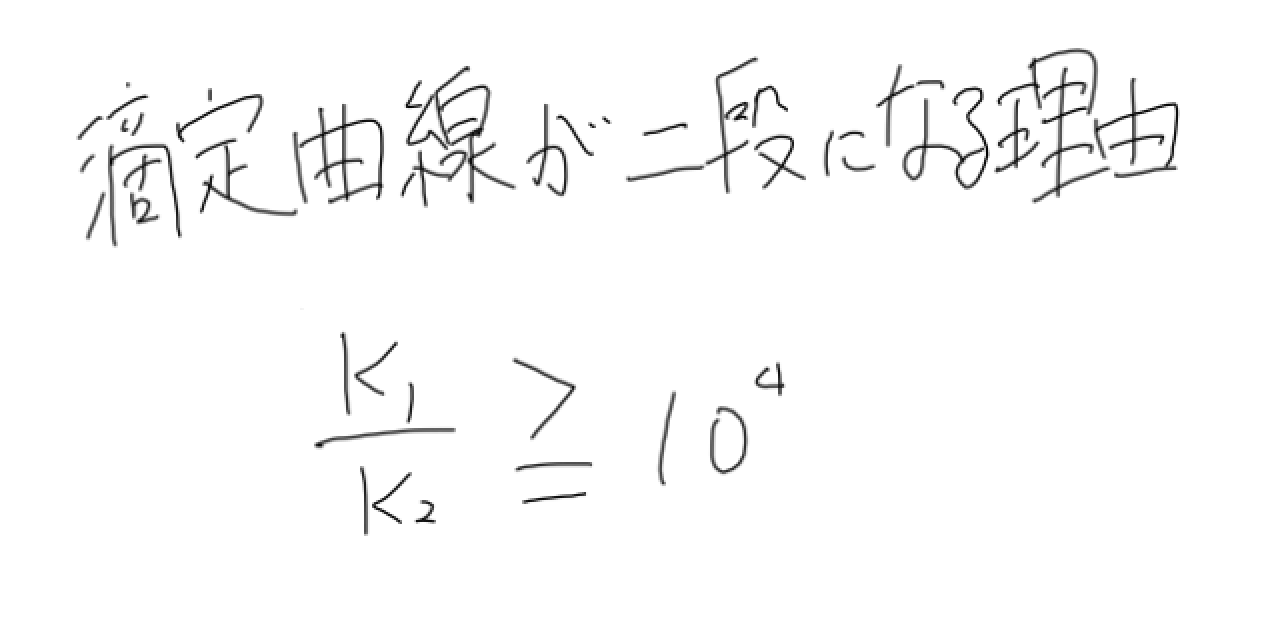
炭酸もそうですよね。
じゃあシュウ酸を見ていきましょう。
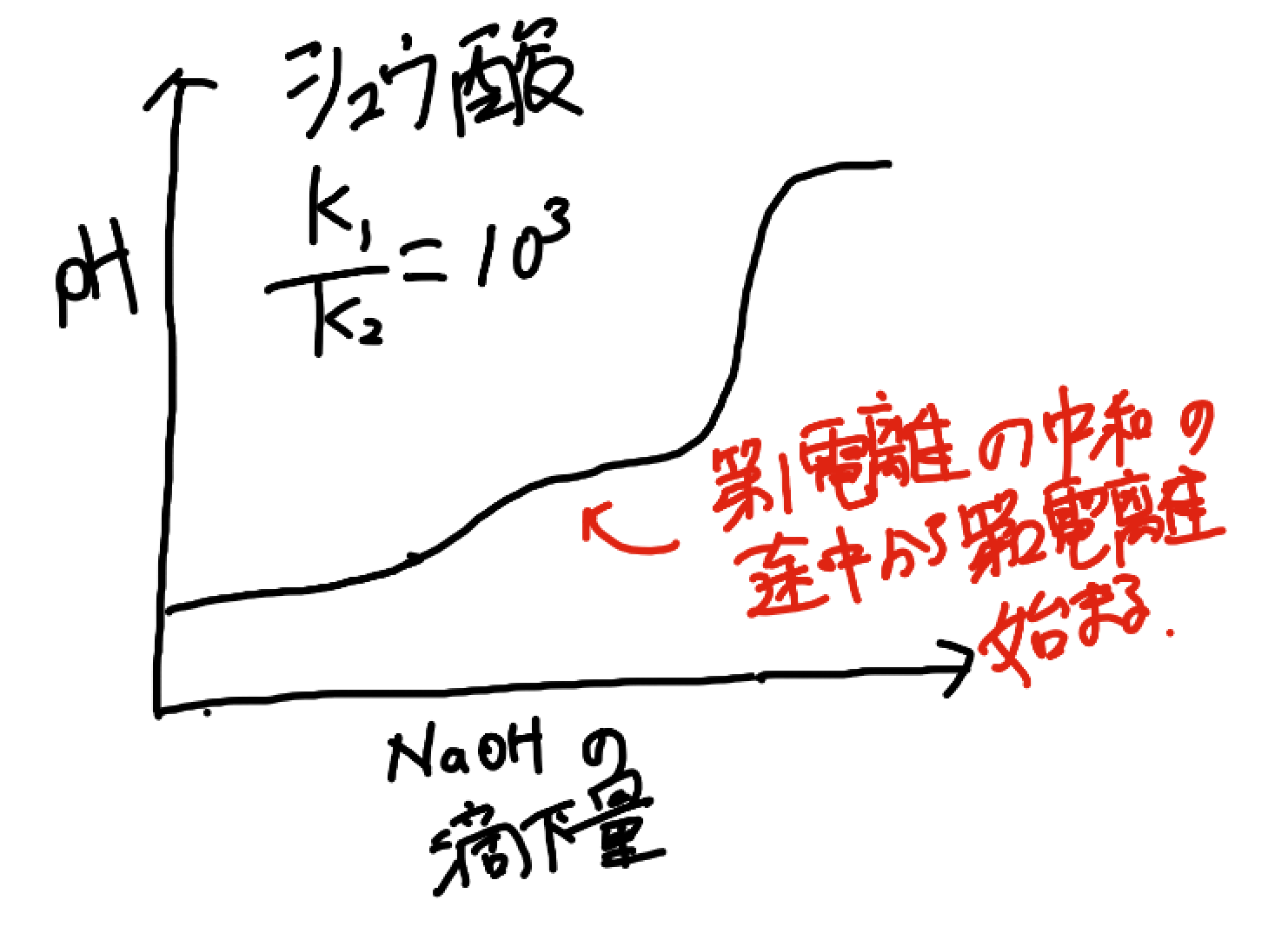
シュウ酸は、
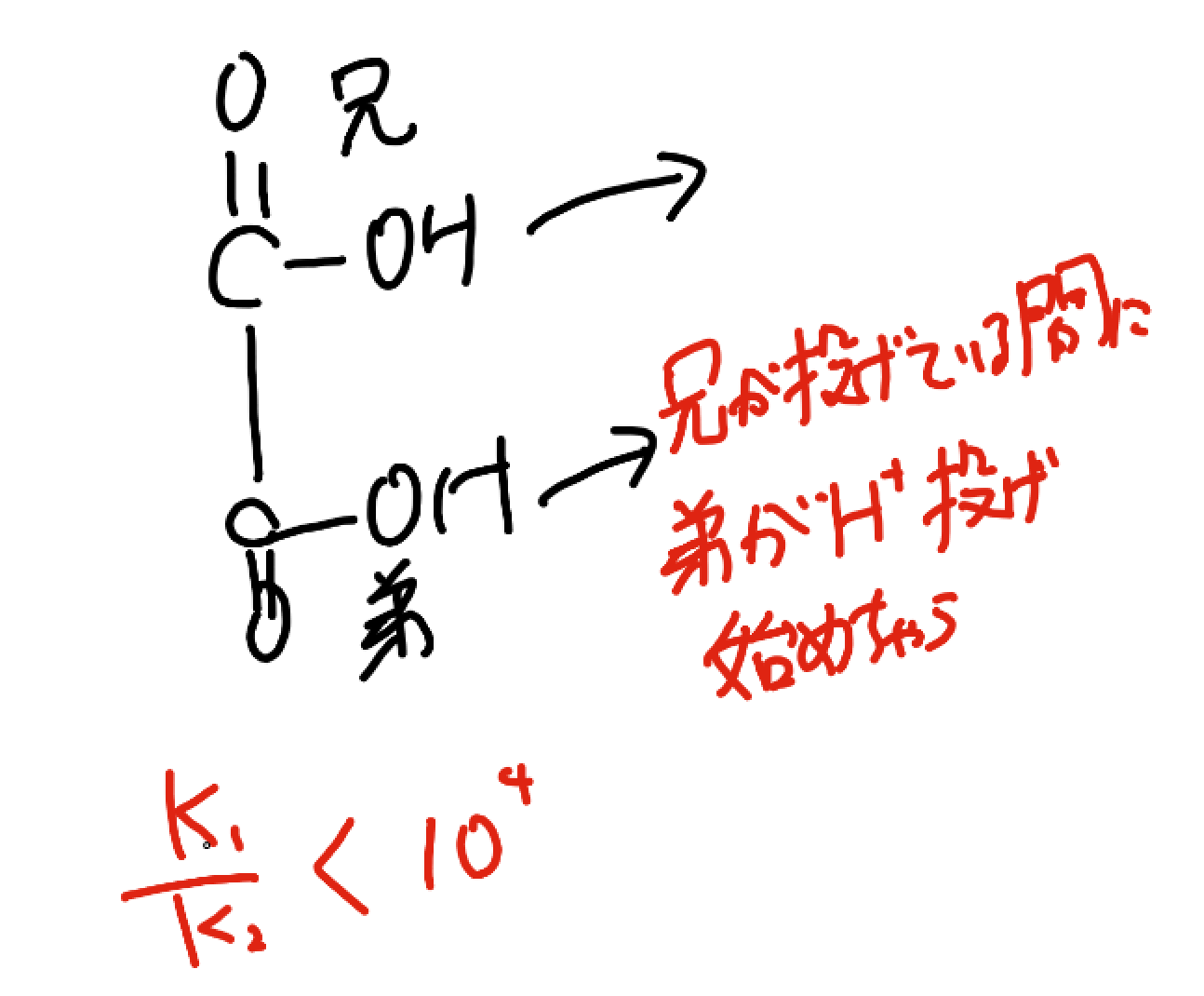
なので二段滴定にはなりません。
硫酸は、そもそも第1電離も第2電離もむっちゃでっかいので、そもそも論外のような中和滴定曲線になっているんです。
大事なのは、二人が別々に投げてくれることなんです。そして二人が別々に投げてくれるかは電離定数の差が
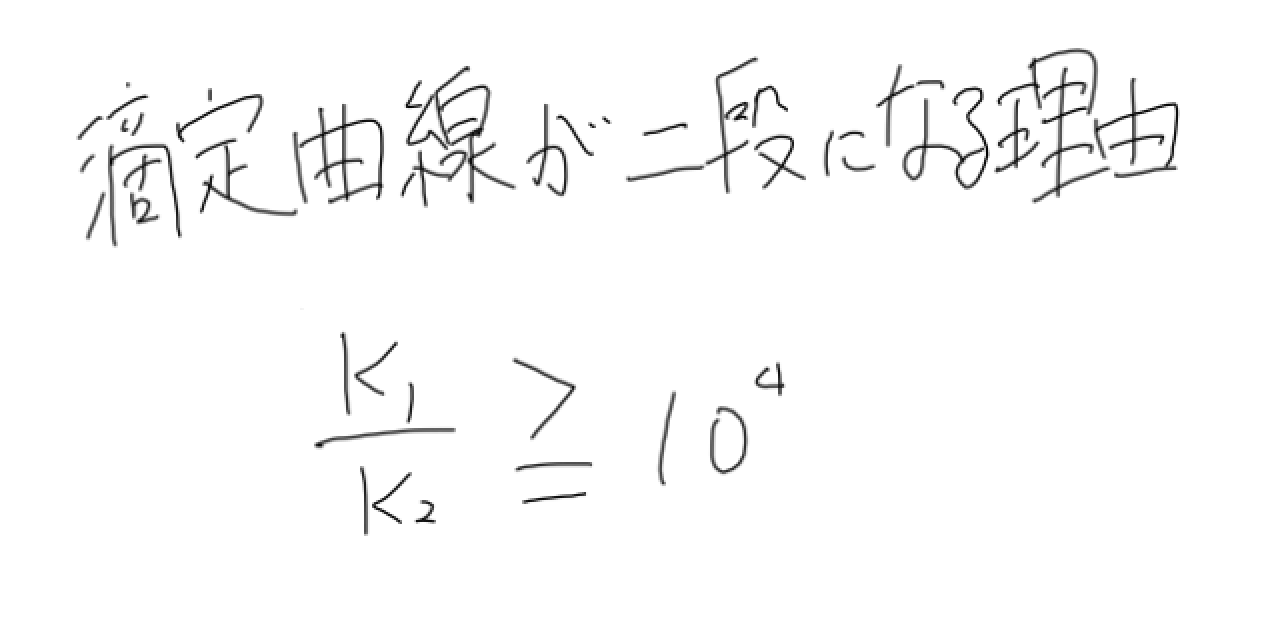
以上になることなんですよ。
補足:二段滴定の滴定開始初期は緩衝液になっている

緩衝液ってのは、強酸や強塩基を少々加えてもほとんどpHが変わらない幻の液(ってほどじゃないけど)のことで詳しくはこちらの記事を読んでください。
この溶液の滴定が始まったときの滴定曲線を見たらわかります。

この時は、弱酸の炭酸と弱酸の塩の炭酸水素ナトリウムができてますよね。よって緩衝液です。どういう時に緩衝液になるかがわからない人はやばいっすよ!ちゃんと確認しといてくださいね!
入試頻出「炭酸ナトリウム」の二段滴定!

ではようやく、二段滴定でもっともよく出る「炭酸ナトリウム」について話していこうかと思いますよ!
なんで炭酸ナトリウムが二段滴定でもっとも試験に出るのか?それは、二段滴定くらいしかまともに入試に出せる奴がいねえから!!
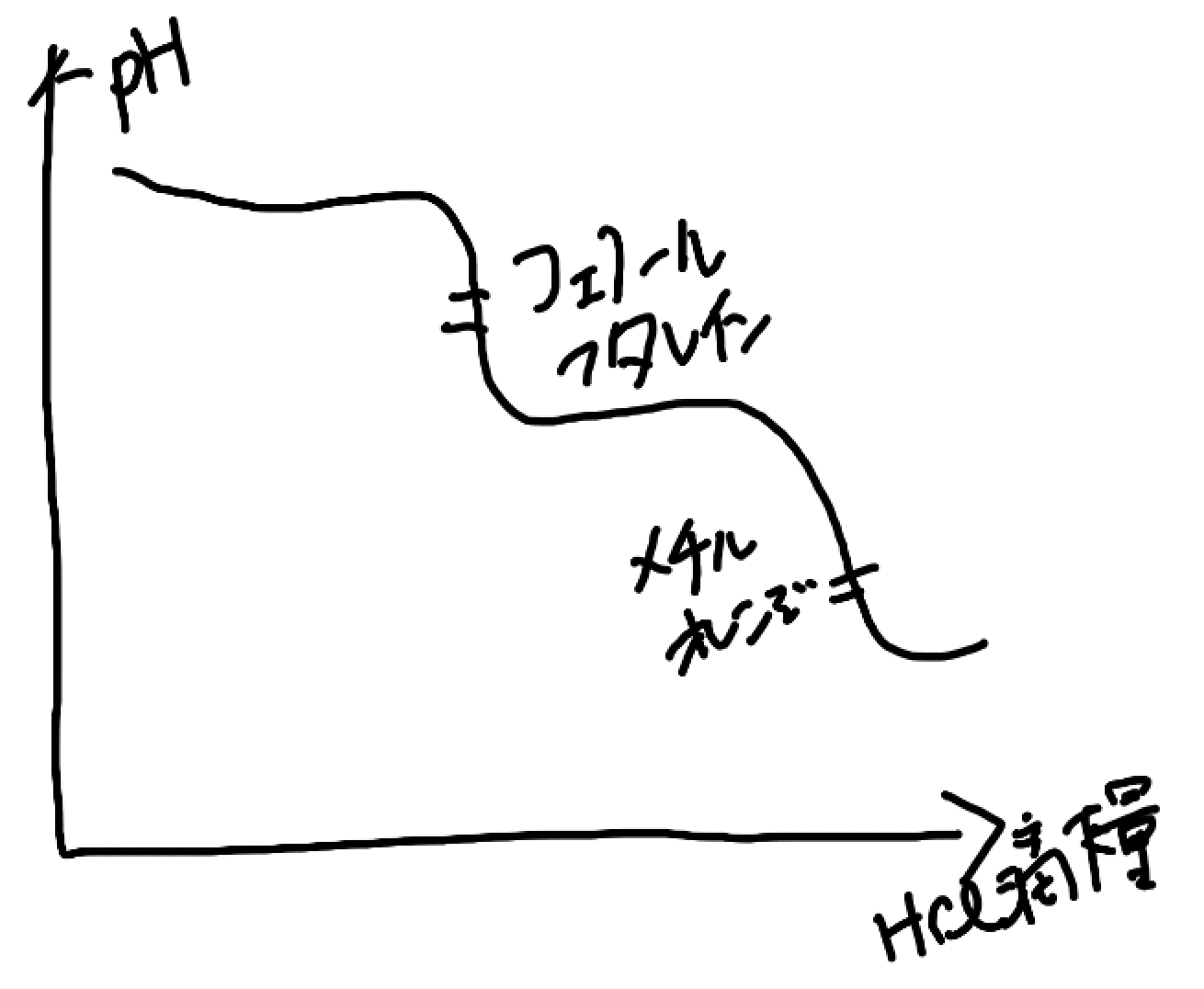
たとえば、炭酸の二段滴定

こういう風になります。すると、、、

第2電離は適した指示薬が存在しないんです。二段目ってpHが大きすぎてフェノールフタレインでは色の変化を検出することができないんですよ。 (7.8~10.0)
で、この変色域がわからないと計算問題を出せないんですよね。2次試験や私立の一般入試ではやっぱり計算問題を出題したいので、きっちり二段とも検出できる炭酸ナトリウムを出題するんですよ。
二段とも検出できる炭酸ナトリウムを出題するんですよ。
だから、検出できるってことは、HClの滴下量がわかるってことですよね。そうするとモル濃度の計算を出題したりしやすいんですよ。あと、炭酸ナトリウムの中和滴定は、水酸化ナトリウムと混ぜて、割と難問にすることができるんです。
ちなみに、今から話す炭酸ナトリウムの二段滴定がわからないと逆滴定(ワルダー法)もわからなくなるので気をつけてくださいね!
ほぼ全てのエッセンスはここまでで話し終えていますので、炭酸ナトリウムに当てはめるだけです。なのでほとんど説明し終えていると言っても過言ではありません。
炭酸ナトリウムの二段滴定の滴定曲線と起こっている反応
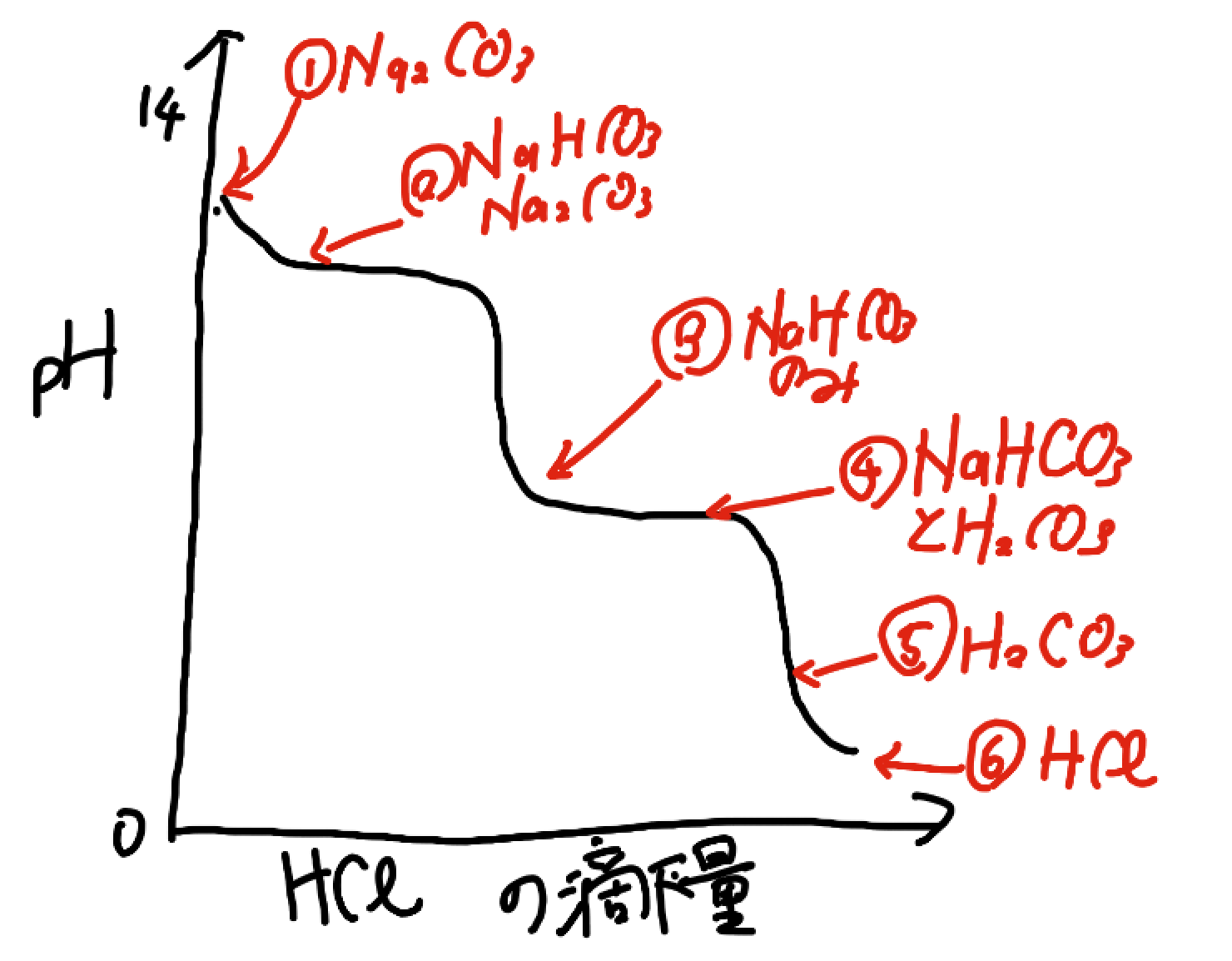
便宜上このように二段滴定を段階分けして6分割しようと思います。
①Na2CO3のみ
炭酸ナトリウムはpH12くらいからだいたい始まりますので、①の場所から始まります。
②NaHCO3とNa2CO3
Na2CO3にHClを滴下すると中和反応が起こります。ちなみにこれを弱酸遊離反応とみることもできます。
Na2CO3+HCl→NaCl+NaHCO3
の反応が起こっています。この反応が完了した時に、1度目のpHジャンプが起こります。指示薬はフェノールフタレインです。
ちなみに、この時も緩衝液です。
③NaHCO3のみ
炭酸水素ナトリウムは炭酸ナトリウムよりも弱塩基ですので、pHも小さくなりますよね。なので、炭酸水素ナトリウムのみの時は、滴定曲線では③の場所になります。
④NaHCO3とH2CO3⑤H2CO3
NaHCO3+HCl→NaCl+H2CO3
このような反応がおきます。また、炭酸は、不安定なのですぐに水と二酸化炭素に分解されて二酸化炭素が空気中へ消えていってしまいます。
H2CO3→H2O+CO2
となります。
この反応が完了した時に二度目のpHジャンプが起こります。この時の指示薬は、メチルオレンジやメチルレッドです。
⑥HCl
滴定が終わった後、HClの影響でpHは小さくなります。
このような反応を起こしながら炭酸ナトリウムは二段滴定をしていくのです。
炭酸ナトリウムはどのように反応しているのか?
まず、ナトリウム塩は、基本的に溶液中で完全に電離しています。なので溶液中ではこういう状態で存在しています。
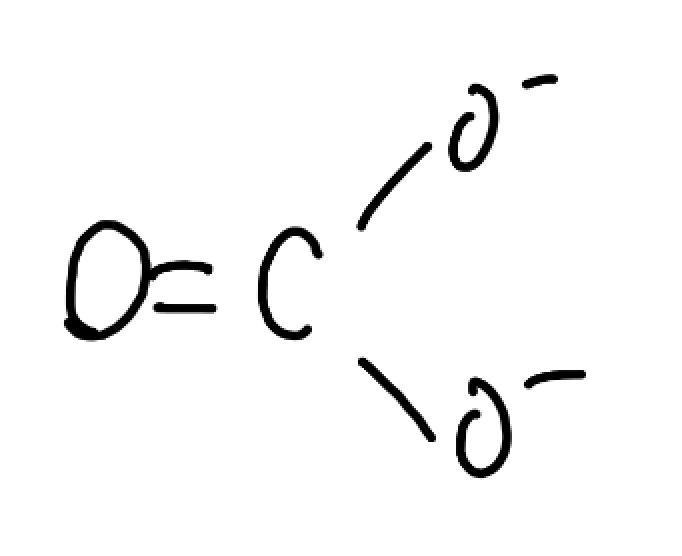
この炭酸イオンがH+を受け取っていく中和反応が起こります。さっきの炭酸の二段滴定と違うところは、炭酸が水素イオンを投げるか受け取るかだけで、ほとんどの何も変わりません。
炭酸ナトリウムが二段滴定になる理由も、兄が水素イオンを受け取り終わってから弟が水素イオンを受け取るからです。ちゃんと順番を守るから二段滴定になるのです。

じゃあ、この弟がちゃんと順番を守るための条件は覚えていますか?
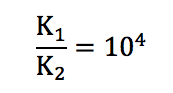
これですよね。
炭酸ナトリウムの反応のイオン反応式は、
CO32–+H+→HCO–3・・・①
HCO–3+H+→H2CO3・・・②
こうなります。1と2の電離定数は、
K1=1010.3
K2=106.3
さっきの電離定数の逆数ですね!
なので、
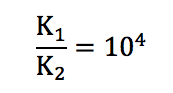
これを満たすので、ちゃんと弟は、兄が水素イオンを受け取り終えた後に、水素イオンを受け取り始めます。
炭酸ナトリウムの二段滴定でどんな問題が出題されるか?
綺麗事抜きで受験生が知りたいのはここのはず。結局何が出るんや?ということが気になりますよね。というかこれしか気にならねえ!って人も。
なので、この二段滴定で一体何が一番重要なのか?ってことを話していきます。ただ、炭酸ナトリウムの二段滴定は、水酸化ナトリウムと炭酸ナトリウムの混合溶液で出ることが多いので、この記事を読み進めたら必ず逆滴定まで読み進めてみてください!
出題ポイントはズバリ!炭酸ナトリウムの1つ目と2つ目の中和に必要なHClの量です。めちゃくちゃ当たり前のことなんです。

当たり前ですよね。
Na2CO3+HCl→NaCl+NaHCO3
NaHCO3+HCl→NaCl+H2CO3
炭酸ナトリウムと炭酸水素ナトリウムのモルが同じなのは大丈夫ですよね。炭酸ナトリウムが炭酸水素ナトリウムになってるんだから当たり前。
そしたら炭酸ナトリウムを炭酸水素ナトリウムに、炭酸水素ナトリウムを炭酸に、滴定完了させるのに必要なHClが同じなのは当然ですよね。
こんな当たり前のことが何に役に立つのか?って思いますよね。これが役に立つんですよ。例えば、炭酸ナトリウムと水酸化ナトリウムが混ざったような滴定だったとします。
NaOHと炭酸ナトリウムは、境界が曖昧なんですよ。その一方、炭酸ナトリウムと炭酸水素ナトリウムは、境界がはっきりしてます。
でも、先ほどの炭酸ナトリウムと炭酸水素ナトリウムのモルが同じっていう関係を使えば、簡単にNaOHを中和するのに必要なHClの滴下量もわかります。
まず、こういう風に変色しますよね。
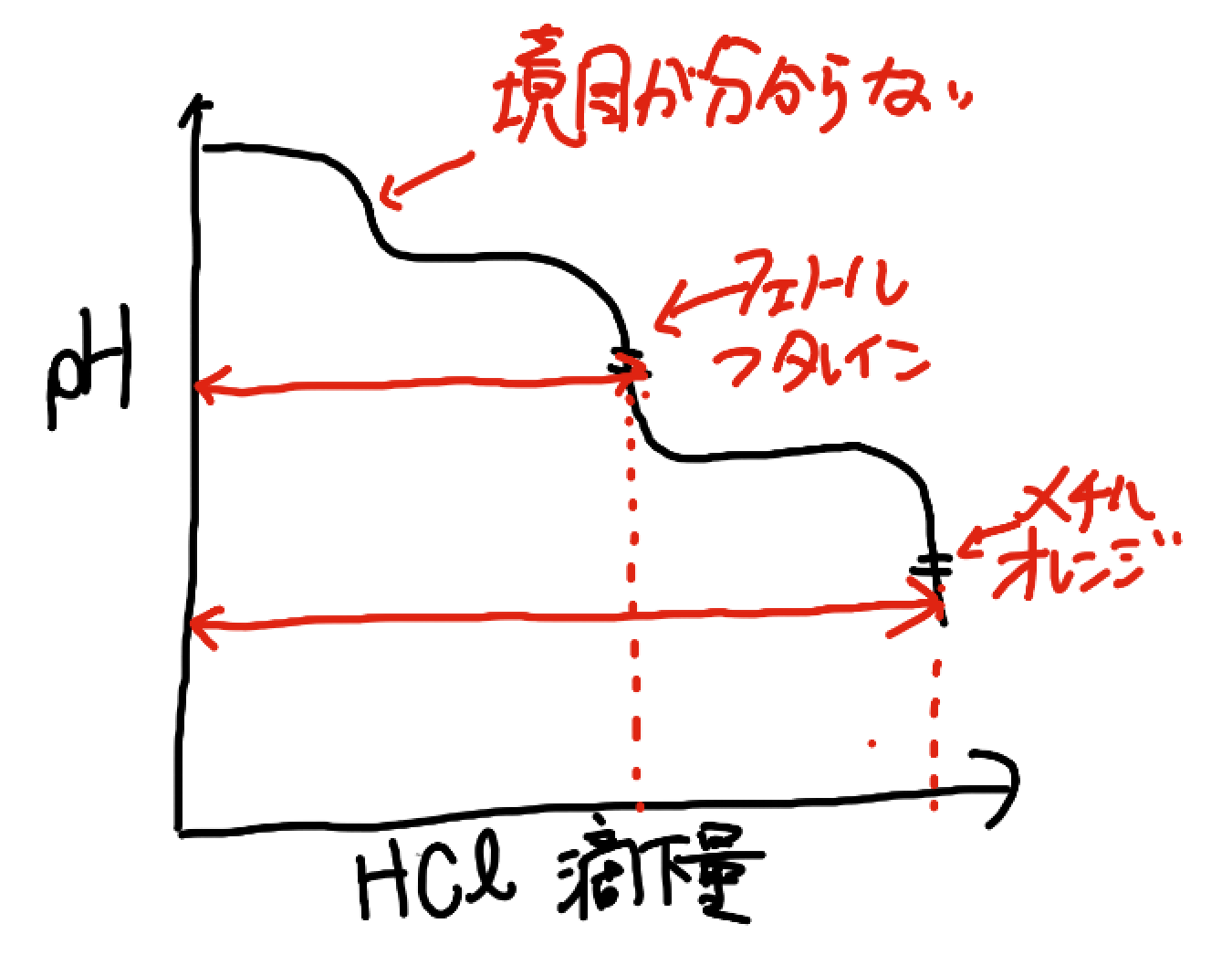
こういう風に、フェノールフタレインとメチルオレンジが変色するのに必要なHClの量、すなわち、炭酸ナトリウム→炭酸水素ナトリウム、炭酸水素ナトリウム→炭酸に中和するのに必要なHClの量がわかります。
そして、炭酸ナトリウム→炭酸水素ナトリウム、炭酸水素ナトリウム→炭酸にするのに必要なHClの量は全く同じなんです。
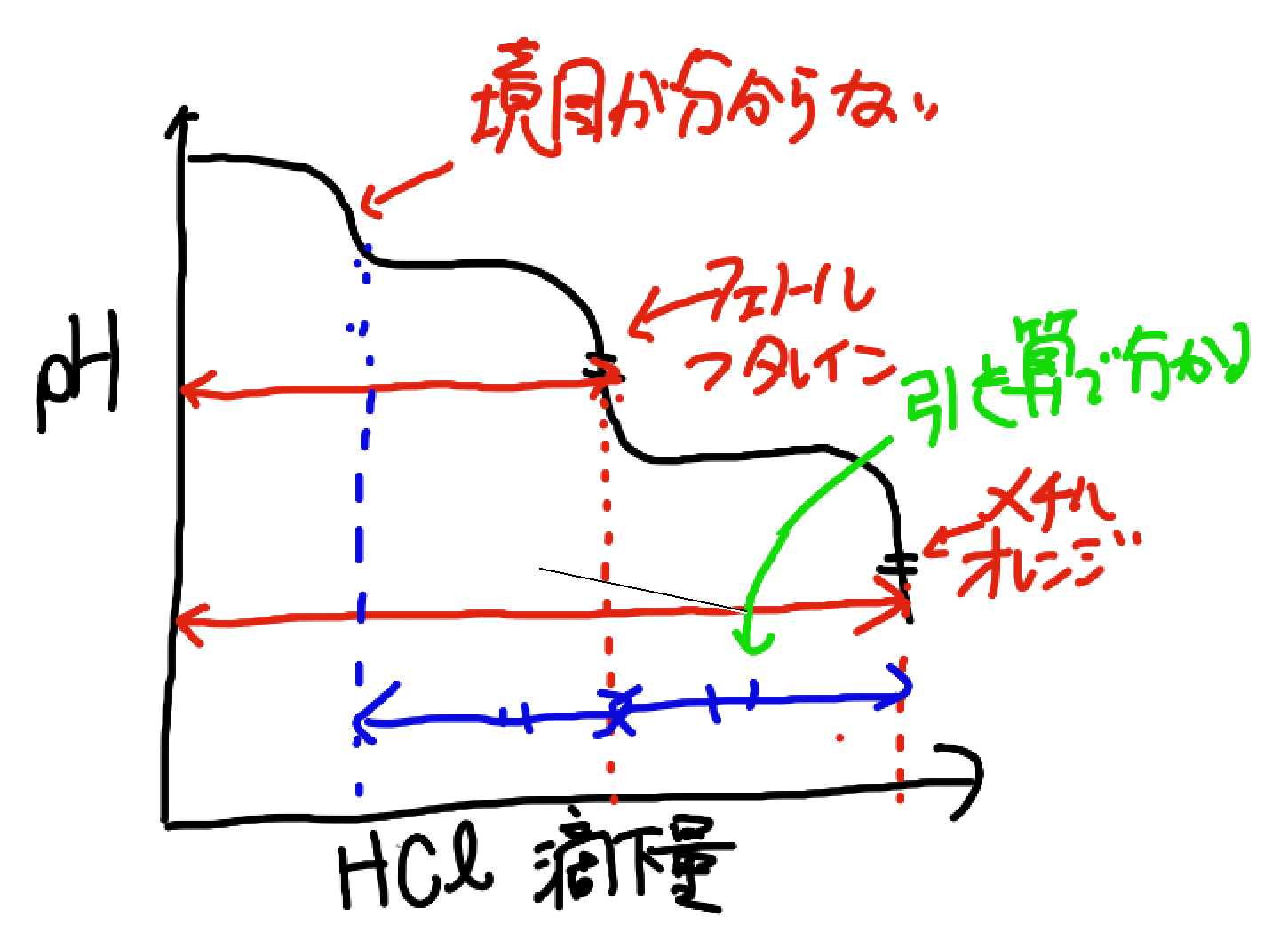
これを使えば、滴定曲線より、NaOHの量がわかります。

滴定開始からメチルオレンジが変色するまでのHClの滴下量をV1、滴定開始からフェノールフタレインが変色するまでの滴下量をV2とすると、
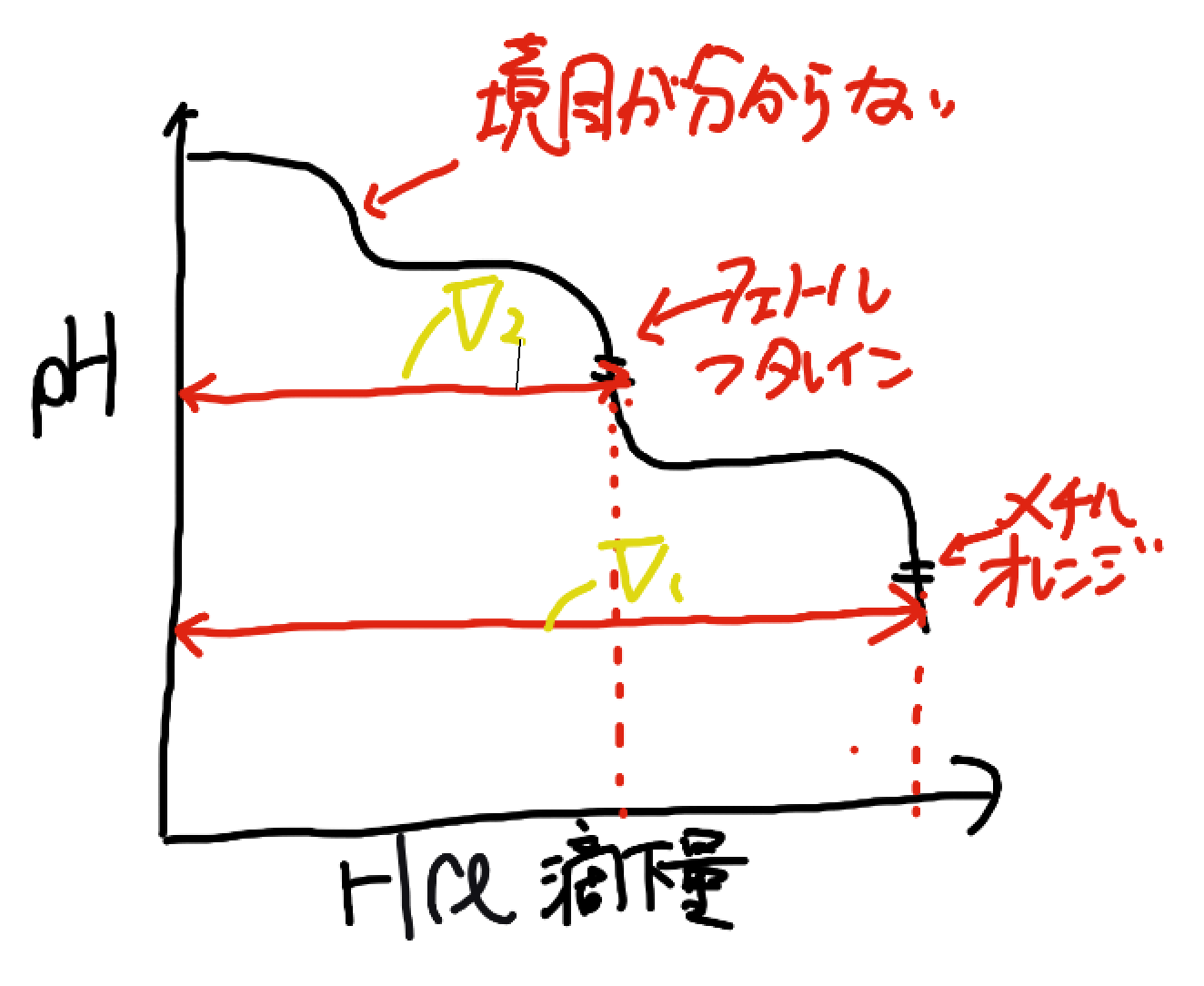
すると、NaOHを中和するのに必要なHClの滴下量をV3とすると、

このようにV3を求めることができます。HClの滴下量がわかれば、NaOHもわかりますからね!
補足
炭酸ナトリウムはソルベー法で工業的に大量生産することができます!
最後に
この炭酸ナトリウムの二段滴定は、NaOHと混ざったときの逆滴定のかませ犬です。こっからが本番です。きっちり逆滴定をマスターしていきましょう!
















CO2 + 2NaOH → Na2CO3 の反応ですが、
H原子はどうなるのでしょうか?
誤植ですね。ありがとうございます。
学校で重問の二段滴定の解説を受けたのですが、全く理解できずに挫けそうになってました。
しかし、このブログを見て二段滴定をしっかり理解することができました!重問の問題も炭酸ナトリウムの二段中和を段階を踏んで考えることができました☆本当にありがとうございますm(*_ _)m
これからもこのブログを活用させていただきながら頑張ります!!
ありがとうございます!メチャクチャうれしいです!
是非どんどん活用していってください!
なんで炭酸ナトリウムを使ってCO2の逆滴定になるのかがやっと理解できました!
本当にありがとうございます!
ありがとうございます!
はじめまして。
コメントするのは初めてですが、いつも参考にさせてもらってます。
そこで質問なのですが、最後の物質量の算出にある滴定曲線において同じYmolになる、ということは最初から炭酸ナトリウムは2Ymolあるということなのでしょうか?
いえ、違います。炭酸ナトリウムは2本手があるので、炭酸ナトリウムが1mol在ったとしたら、炭酸に戻すためには2mol必要ということです。
H2分子1molあればH原子は2molだよね。
っていう話と一緒です。
なるほど!
納得できました!ありがとうございます!
学校でした時は全く解けなかったけど、これを見て簡単に理解できました!今年は受験しますが、受験化学を頑張ろうと思いました。
NaOHがNa2CO3よりも先にHClと反応するのは何故ですか?
強塩基ゆえ
やっと理解したぜ!