化学基礎で最初の方に習う基礎的な内容の「組成式」と「分子式」ですが、意外とその違いが見分けづらいです。
例えば、CO2は分子式でSiO2は組成式です。もちろん、わかる人には当たり前なんですが、わからない人にとってはなかなか厳しい内容です。
また、組成式は金属結晶やイオン結晶を表すためのものだと思っています。そのような間違った認識をしている人のために、今回組成式と分子式の違いをバッチリ解説しました。
目次
ズバリ!組成式と分子式の違いは?
組成式=物質の構成原子とその数の比
分子式=分子の構成原子とその数
組成式の英語は、Comparison(比) Formular(式)です。そのまんま比の式なんです。一方で、分子式の英語は、Molecular(分子) formular(式)です。そのまんま分子の式なんです。
なので、

ここで、多くの人が勘違いを正しておきましょう。
分子にだって、共有結合の結晶にだって、組成式は存在します。
例えば、A100000000000B200000000000っていう分子があったとします。これを分子式と組成式で表すとすると、
分子式ならば、A100000000000B200000000000で構成原子の数をそのまま表すので、これが正解です。一方で、組成式は、原子の数の比ですので、AB2と省略することができます。
また、このことから
分子式=(組成式)n
と表すことができます。
例えば、グルコースはC6H12O6=(CH2O)6ですので、分子式はC6H12O6で組成式はCH2Oです。
分子式はその名の通り、分子の実態を表すためのものです。組成式は化学式で表せるものには全て使えます。
よくある勘違いで、組成式は金属結晶やイオン結晶に使うものと暗記している人もいますが、そうではなく分子だとしても組成式は表せます。
組成式と分子式の違いを記述問題で聞かれた場合は、次のように答えておけばいいでしょう。
組成式は構成原子と原子数の整数比を表し、分子式は分子を構成する原子とその数を表す。
組成式と分子式の違いがわかりにくいもの

と人々が声をあげて驚くのが、SiO2でしょう。
見た感じ、CO2とそっくりだし、SiとCって14族元素で、同じような性質を持っていますよね。なので、二つとも分子じゃないの? って思ってしまうでしょう。
ですが、SiO2はCO2と違って、超巨大な高分子です。SiO2の実態は下のような感じです。

なので、共有結合の結晶たちは、組成式で表します。これは、分子結晶と共有結合の結晶の違いを書いた記事でも解説しました。分子なのか共有結合の結晶なのかの区別はつけられるようにしておきましょう。
練習問題
グルコースの組成式と分子式を求めよ。
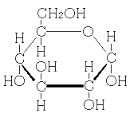
C:H:O=6:12:6=1:2:1と表せます。よって、組成式はCH2Oとなります。
次の物質を化学式であらわしたとき、組成式であらわされる物質はどれか。
1)黒鉛 2)ヨウ素 3)塩化ナトリウム 4)アンモニア
まず、1)は、黒鉛です。黒鉛は分子ではなく共有結合の結晶です。もし分子式で本気で表すなら、黒鉛のCの数を全て数えなければなりません。C144527402584とかになるかもしれませんね。現実的ではないので、組成式で表します。
3)は、イオン結晶ですので、組成式で表します。
まとめ
てな訳で、組成式と分子式の違いをまとめると。
組成式=物質の構成原子とその数の比
分子式=分子の構成原子とその数