こんにちは。
濃度平衡定数と圧平衡定数について
お話しします。
化学平衡状態というのは、
熱化学的に非常に安定な状態、
というのは、以前お話しました。
目次
化学平衡の法則(質量作用の法則)
化学平衡の法則(質量作用の法則)は、
2つの記述のしかたが、あります。
それこそ、
濃度平衡定数と圧平衡定数
なんだが、、、
その濃度と圧力の2つの書き方を
学んで行きましょう!
濃度を用いた表現、濃度平衡定数
A2+B2⇄2AB
という平衡反応があります。
物質A2,B2,ABの
それぞれのモル濃度[A2][B2][AB]
のあいだには、次の関係式が成立します。
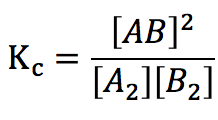
この式で表される関係を、
化学平衡の法則または、
質量作用の法則といい、ここで、
KC(cは濃度:Concentration)
で平衡定数と呼びます。
普段では、これは、
KCで表される事は無く、
K=KCのことだと
思って良いです。
圧力を用いた表現圧平衡定数とは
次の反応がある温度で平衡状態のとき、
A2(気)+B2(気)⇄2AB(気)
このとき、
気体A,B,ABの分圧を、
PA,PB,PABと
あらわされるとき、
この3つの気体には、
次の関係式が成り立ちます。
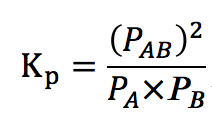
この式で表される関係の事を
先ほどと同じように、
化学平衡の法則、
または質量作用の法則
と言います。
これも、温度に依存しますが、
圧力や濃度には依存しません。
この定数を圧平衡定数と言います。
平衡定数と反応速度定数の関係
H2+I2⇄2HI
という反応があったとします。
この反応で、
左から右(正反応)の反応速度式は、
v1=k1[H2][I2]
右から左(逆反応)の反応速度式は、
v2=k2[HI]2
となります。
で、平衡状態というのは、
正反応と逆反応の反応速度が、
同じ状態でした。
よって、平衡定数を反応速度定数で
表すと、

となります。
これの覚え方ですが、
『正/逆』です。
「逆分の正」「逆分の正」「逆分の正」
と唱え続けてください!
濃度平衡定数と圧平衡定数の関係
次の化学平衡の反応が起っている、
とします。
wW(気体)+xX(気体)+・・・・⇄yY(気体)+zZ(気体)+・・・
濃度平衡定数KCと
圧平衡定数KPについて、
次の関係式が成立します。
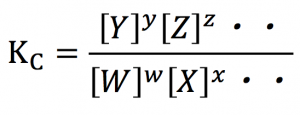
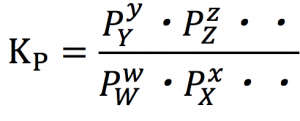
そして、ここで、
この2つの関係を見てみましょう!
状態方程式、PV=nRTを変形し、
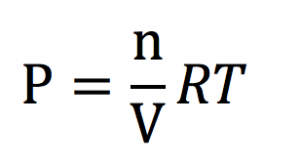
このn/Vがモル濃度なので、
先ほどの分圧をモル濃度で、
表す事ができます。
Pw=[W]RT
PX=[X]RT
PY=[Y]RT
Pz=[Z]RT
となります。
これを圧平衡定数に代入すると、
圧平衡定数と濃度平衡定数の関係を
付ける事が出来ます。

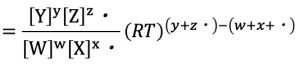

のようになります。
また、H2+I2⇄2HIのような、
『左辺、右辺のそれぞれの
係数の総和が等しい場合』
は、
KC=KP
が成り立ちます。
可逆反応とは?
平衡定数を決める事が出来ると、
可逆反応とは、何か?が
説明できます。

可逆と言うのは、
『両辺生き残る』
+
『平衡定数一定』
と覚えてください。
両辺に、残ると言う事を
利用しているのが、
塩の加水分解です。
平衡定数の問題の解き方のステップ
化学平衡の計算というのは、
(電離平衡がちょっと例外的ではあるが、)
この2ステップで解く事が出来ます。
なので、この2つを意識してください!
それでは、全体的な、
2ステップの解法をお教え
します。
ステップ①モル収支表を書く

モル収支表というのは、
勝手にワタナベが命名したので、
一般的に通じる言葉ではありません。
ですが、
反応でモルがどのように変化するか、
その収支を表にまとめてあるので、
モル収支表と呼んでいます。
これは、モル計算でも
気体の分野でもよく使うので、
キッチリ使えるようにしておいてください。
ステップ②平衡定数一定式

平衡定数というのは、
温度一定なら一定です。
なので、温度が変わらなければ、
常にその反応で一定です。
だから、何かを足しても、
一定ですし、
圧力が変わっても
一定です。
なので、モル収支表を書いて、
新しい平衡状態でも、
K一定の式を立てます。
計算が面倒な問題も多く
ありますが、それは覚悟してください。
基本的に、解法でつまづく事は
あまり無い分野です。
例題
では実際にこの解法を使いこなして行きましょう!
例題を出して行こうと思います。
CH3COOH+C2H5OH⇄CH3COOC2H5+H2O
問1 上記の平衡反応の平衡定数Kを整数で求めよ。
問2 20℃で酢酸2molとエタノール1molを混ぜると、平衡状態で何モルの酢酸エチルが生成するか。ただし、√2=1.41,√3=1.73とし、有効数字2桁で答えよ。
この問題を解いて行きます。
ステップ①収支表を書く
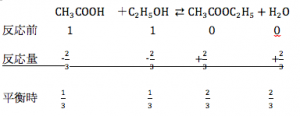
このように収支表を書きます。
ステップ②K式一定条件
そしてこれをK一定と連立します。

これより平衡定数K=4となります。
問2
またまた同様に解いて行きましょう
ステップ①収支表を書く

このようにモル収支表を
書きます。
ステップ②K式一定条件
先ほど求めた、
平衡定数一定条件を
使えば、

これより、xについて整理すると、
3x2-12x+8=0
ちなみに、このxは反応量
だから、負の可能性はない、
さらに、エタノールが1molしか
ないため、反応量が1molを
超える事も無い。
よって、0<x<1という
条件がわかる。
よって、これをとくと、

x=0.846mol
解答は
問1 4
問2 8.5×10-1mol
です。
平衡定数を扱う裏技的方法
分子の変数をすっきりしたいと言うもの、
なので、初期状態を全て、
平衡定数を扱う裏技的方法














例題の問2で「酢酸2molとエタノール2molを混ぜた」とありますが解説を見ると酢酸2molとエタノール1molになっているのですが、誤植でしょうか。
修正しましたすみません。
なぜ収支表で濃度に電離度をかけるんですか?
学校で酸の電離定数を公式(Ka=cα^2)という形で覚えさせられたのですがモル収支表を書かずに公式にぶっこむのは危険ですか?
危険です!