こんにちは。
酸化還元滴定って、わかるようでわかりにくいですよね。中和滴定に似ているようで、少し違います。また、酸塩基の中和滴定ならば、
酸のH+mol=塩基のOH-mol
と立てる計算式も明確でしたよね。でも酸化還元滴定になると、どんな式を立てたらいいのかわからなくなりますよね。
てな訳で、今回の記事では酸化還元滴定の初歩の初歩から、たった2パターンしかない酸化還元滴定の計算方法まで全てがわかるようになっています。
なので、永久保存版として、この記事をなんども読みこなしていってください。
- 酸化還元滴定とは?
- 酸化還元滴定の計算はどんな式を立てる?
- 酸化還元滴定のたった2つのパターンとは?
- 具体的に過マンガン酸塩滴定のやり方は?
目次
酸化還元滴定とは?
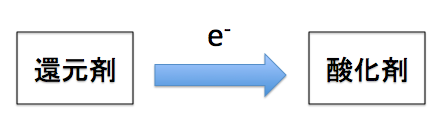
酸化還元反応 定義
これが、酸化還元の最重要定義でした。還元剤が電子を投げて酸化剤が電子を受け取る。
すると、1つの式を作り出すことができます。
還元剤が投げた電子のモル=酸化剤が受け取った電子のモル
この関係式を使って酸化剤または還元剤の濃度を計算で求めていきます。
今回は、酸化還元滴定の超有名パターン過マンガン酸塩滴定で酸化還元滴定の詳しい実験方法や、計算方法、入試問題で出題される記述問題などを解説していきます。
もう1つのパターンはヨウ素を使った「ヨウ素滴定」です。
過マンガン酸イオンを用いた酸化還元滴定の流れ
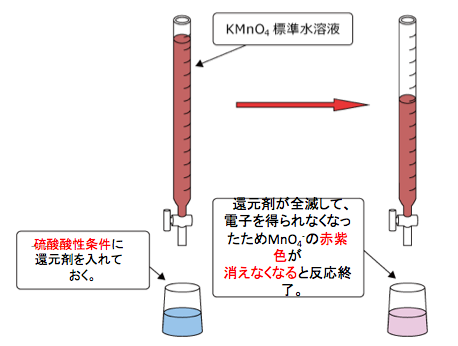
今回の酸化還元滴定では、ビュレットから滴定する溶液が過マンガン酸イオン、滴下されるビーカーにシュウ酸溶液とします。下のような感じ。
.jpg)
酸化還元滴定開始初期〜ビーカーの中身が シュウ酸>過マンガン酸イオン〜
過マンガン酸イオンを徐々に滴定していくので、どうしても最初はシュウ酸が多く、過マンガン酸イオンが少ない状態になりますよね。

まず、シュウ酸に過マンガン酸イオンを滴下すると、シュウ酸が滴下されたMnO4–を酸化還元反応でMn2+にします。

すると、最初は少量のMnO4–しかないのですぐにシュウ酸に食いつぶされてしまいます。

なので、この段階での溶液の色は無色透明です。
酸化還元滴定開始後期〜ビーカーの中身がシュウ酸<過マンガン酸イオン〜
最初の方は滴下された過マンガン酸イオンは全てシュウ酸と反応していました。
しかし、徐々に反応が進むと、徐々にビーカーの中のシュウ酸が消えていきます。そして最終的には、シュウ酸の量関係が逆転する瞬間が訪れます。それが滴定の終点で、「当量点」と言われます。

このように、シュウ酸が駆逐されると、赤紫色のMnO4–を打ち消そうとするものがいなくなりますよね。てことは、赤紫色が消えなくなるのです。
つまり、過マンガン酸イオンを使って滴定は、当量点(滴定終了地点)を「過マンガン酸イオンの赤紫色が消えなくなった時点」で判断します。
これめちゃくちゃ重要です。酸化還元滴定の問題では必ずと言ってもいいほど必ず出題されます。
「実験における滴定の終点は、どのように判定されるか。」と聞かれます。なので記述問題では、
滴下する過マンガン酸カリウム水溶液の赤紫色が消えなくなるところを終点とする
とバッチリ答えてあげればいいでしょう。
酸化還元滴定滴定の計算法を演習問題で学んでみよう
てな訳で、理論化学なので、計算問題からは逃げられません。多くの人は化学反応式を立てて計算しようとするのですが、これは非常に勿体無いやり方です。
わざわざ化学反応式を作る必要はありません。モル比さえわかればいいのです。理論化学の計算は「モル利用」「モル比」からぶれて単元ごとに解法を変えてはいけません。
この時の過マンガン酸カリウムのモル濃度を求めよ。
てな訳で、問題を解いていきます。
ステップ1:半反応式を確認する
まずは、半反応式から確認していきますね。
還元剤:(COOH)2→2CO2+2H++2e–
酸化剤:MnO4–+5e–+8H+→4H2O+Mn2+
この2つになります。
ステップ2:酸化剤、還元剤のモルを求めてそれらを等号で結ぶ
酸化還元の定義通りに式を作ります。
「還元剤が投げた電子のモル=酸化剤が受け取った電子のモル」
という式を作ります。
0.756÷126×2×10/100=0.012mol=1.2mmol
次に過マンガン酸イオンが受け取る電子のモルを求めます。求めるのがこの過マンガン酸イオンのモル濃度なので、これをCと未知数でおきます。
C×16.00×5=80C
てことで、これらを等号で結びます。
ステップ3:方程式を解く
普通に方程式をときます。
80C=1.2
∴C=0.015mol/L
となります。
このように
なぜ硫酸酸性条件にするのか?
酸化還元滴定で、なぜ「硫酸酸性条件にするのか?」ってことが記述問題で問われたりします。
なぜ酸性条件が必要なのか?
これは、MnO4–の酸化剤としての性質のせいです。MnO4–は酸化剤の半反応式って2パターン存在したのはご存知ですか?
(酸性条件)MnO4–+5e–+8H+→4H2O+Mn2+
(中性条件)MnO4–+4H++3e–→MnO2+2H2O
ですよね。そして、この過マンガン酸イオンを使った酸化還元滴定で最も重要だったのが、「過マンガン酸イオンの色」でしたね。
過マンガン酸イオンの赤紫色が「消えなくなる」というのが重要でした。Mn2+は無色ですが、MnO2は褐色です。下の画像が酸化マンガンです。

色がついているため、酸化マンガンだと終点がぼやけてしまいます。よって、硫酸酸性で確実にMn2+(無色)まで変化させる必要があるのです。
なぜ硫酸なのか?
この滴定では、上の理由から強酸にしておく必要があります。じゃあ、強酸だったら硝酸でもいいし、塩酸でもいいはず。なんで硫酸なんでしょうか?
それは、硝酸だと
NO3–+3e–+4H+→2H2O+NO
このように酸化剤として働いてしまいます。また、塩酸だと
2Cl–→Cl2+2e–
のように、還元剤として働いてしまいます。てな訳で、
一方、希硫酸は酸化力を持ちません。硫酸が酸化還元反応をするのは、加熱して熱濃硫酸になった時だけです。てな訳で、滴定の量計算に影響を及ぼさないのが硫酸なのです。
もし塩酸や硝酸を使ってしまったら、酸化還元反応の量関係が崩れてしまいますからね。
まとめ
- MnO4-は赤紫色、MnO2は褐色、Mn2+は透明
- 過マンガン酸イオンを使った酸化還元滴定は赤紫色が消えなくなったときが終点
- 計算式は「還元剤が投げた電子のmol=酸化剤が受け取った電子のmol」
- 硫酸酸性にする理由はかけるようにしておく
今日の記事はいかがでしたか?
最後までご覧いただきありがとうございました。














こんにちは!
酸化還元滴定がすごく簡単に溶けるようになりました。本当にありがとうございます!
かなり初歩的で恥ずかしいのですが…。
演習をしている間によく分からなくなりました。
中和滴定と酸化還元滴定の計算の仕方の違いが分かりません。
中和滴定では「酸の価数×物質量=塩基の価数×物質量」、酸化還元滴定では化学反応式から計算を進めていくのでしょうか?
問題文の誤字が多かったので修正していだだけると有難いです。
了解